��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ŷ��ԭ����2012��1��1�������պ���̼��˰��Ӧ�Ա����ڻ���ȫ���ů��ʹ�ö���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������̼��Դ���о��Եø��ӽ��ȡ�����?�û�ѧ��Ӧԭ�������֪ʶ�о�̼���仯��������ʡ�
��1�����������ҹ���������̼���о�ȡ���ش��չ���õ绡���ϳɵ�̼�����г����д���̼�����������ʣ�������̼���������������������ᴿ���䷴Ӧ�Ļ�ѧ����ʽΪ��
____C?+?____K2Cr2O7?+?____��?____CO2��+?____K2SO4?+?____Cr2(SO4)3?+?____H2O
����ɲ���ƽ������ѧ����ʽ��
��2���״���һ������ȼ�ϣ��״�ȼ�ϵ�ؼ�����ʵ��������ҵ����������ҵ��һ����CO��H2Ϊԭ�Ϻϳɼ״����÷�Ӧ���Ȼ�ѧ����ʽΪ��CO(g)+?2H2(g) CH3OH(g)??��H1����116?kJ/mol
CH3OH(g)??��H1����116?kJ/mol
�����д�ʩ������������÷�Ӧ�ķ�Ӧ���ʵ���??_______��
A����ʱ��CH3OH�뷴Ӧ��������???????
B�����ͷ�Ӧ�¶�????
C��������ϵѹǿ??????????????????????????
D��ʹ�ø�Ч����??
����֪��
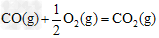 ?��H2����283?kJ��mol-1???????
?��H2����283?kJ��mol-1???????
 ?��H3����242?kJ��mol-1
?��H3����242?kJ��mol-1
���ʾ1mol��̬�״���ȫȼ������CO2��ˮ����ʱ���Ȼ�ѧ����ʽΪ______________��
�����ݻ�Ϊ1L�ĺ��������У��ֱ��о���230�桢250���270�������¶��ºϳɼ״��Ĺ��ɡ���ͼ�����������¶��²�ͬ��H2��CO����ʼ��ɱȣ���ʼʱCO�����ʵ�����Ϊ1mol����COƽ��ת���ʵĹ�ϵ��
��ش�:

���������������¶��У�����Z��Ӧ���¶���___________________��
��������ͼ��a���Ӧ�����ݣ����������Z �ڶ�Ӧ�¶���CO(g)+?2H2(g)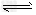 CH3OH(g)?��ƽ�ⳣ��K?=__________��
CH3OH(g)?��ƽ�ⳣ��K?=__________��
��3��CO2����Ȼ��ѭ��ʱ����CaCO3��Ӧ��CaCO3��һ���������ʣ���Ksp=2.8��10-9��CaCl2��Һ��Na2CO3��Һ��Ͽ��γ�CaCO3�������ֽ��������CaCl2��Һ��Na2CO3��Һ��ϣ���Na2CO3��Һ��Ũ��Ϊ7��10-4mol/L?�������ɳ�������CaCl2��Һ����СŨ��Ϊ__________��
�ο��𰸣���1��3???2???8H2SO4???3???2???2?
���������
�����Ѷȣ�һ��
2������� t��ʱ����3molA��2molB����ͨ�����Ϊ2L���ܱ�������(�ݻ�����)���������·�Ӧ��3A (g)+B(g)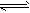 xC(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ��1.8molB�������C��Ũ��Ϊ0.4mol/L��
xC(g)��2minʱ��Ӧ�ﵽƽ��״̬(�¶Ȳ���)��ʣ��1.8molB�������C��Ũ��Ϊ0.4mol/L��
����д���пհף�
��1��v(B) =_________��v(C) =_________��x=_________��
��2���Ƚϴﵽƽ��ʱ��A��B����Ӧ���ת����֮��Ϊ��(A)����(B)��_________��
��3����������ԭƽ�������������ͨ����������(������A��B��C������Ӧ)������˵������ȷ����
____________(��д��ĸ���)
A����ѧƽ��������Ӧ�����ƶ�
B����ѧƽ�����淴Ӧ�����ƶ�
C����ѧƽ�ⲻ�ᷢ���ƶ�
D�������淴Ӧ�Ļ�ѧ��Ӧ���ʱ��ֲ���
�ο��𰸣���1��0.05 mol/(L��min)��0.2 mol/(L
���������
�����Ѷȣ�һ��
3������� ��14�֣�ú��һ����Ҫ�Ļ���ԭ�ϣ����ǽ�����ú��ȡ��ˮú������̿�����ѵȹ㷺���ڹ�ũҵ�����С�
��1����֪:
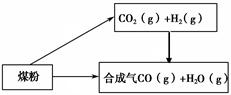
��C(s) �� H2O(g) === CO(g)��H2(g) ��H����131.3 kJ��mol��1
��CO2(g) �� H2(g) ===" CO(g)" �� H2O(g) ��H��+41.3 kJ��mol��1
��̼��ˮ������Ӧ���ɶ�����̼���������Ȼ�ѧ����ʽΪ ��
�÷�Ӧ�� ������¡��������¡����κ��¶ȡ����������������Է����С�
��2����������̿��ԭ�������������������ӦC(s)+2NO(g)  N2(g)+CO2(g)����ij�ܱ������м���һ�����Ļ���̿��NO����T1��ʱ����ͬʱ���ø����ʵ�Ũ�����±���ʾ��
N2(g)+CO2(g)����ij�ܱ������м���һ�����Ļ���̿��NO����T1��ʱ����ͬʱ���ø����ʵ�Ũ�����±���ʾ��
ʱ��(min)
Ũ�ȣ�mol��L-1��
| 0
| 10
| 20
| 30
| 40
| 50
|
NO
| 1.00
| 0.68
| 0.50
| 0.50
| 0.60
| 0.60
|
N2
| 0
| 0.16
| 0.25
| 0.25
| 0.30
| 0.30
|
CO2
| 0
| 0.16
| 0.25
| 0.25
| 0.30
| 0.30
��10��20min�ڣ�N2��ƽ����Ӧ����v(N2)�� ��
��30 min��ֻ�ı�ijһ��������Ӧ���´ﵽƽ�⣬�����ϱ��е������жϸı������������ (����ĸ���)��
A��ͨ��һ������NO B������һ�����Ļ���̿
C��������ʵĴ��� D���ʵ���С���������
��3���о���������ӦCO(g)+H2O(g)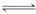 H2(g)+CO2(g)ƽ�ⳣ�����¶ȵı仯���±���ʾ�� H2(g)+CO2(g)ƽ�ⳣ�����¶ȵı仯���±���ʾ��
�¶�/��
| 400
| 500
| 800
| ƽ�ⳣ��K
| 9.94
| 9
| 1
����Ӧ��500��ʱ���У�����ʼʱCO��H2O��Ũ�Ⱦ�Ϊ0.020 mol��L-1���ڸ������´ﵽƽ��ʱ��CO��ת����Ϊ ��
��4����CO��ȼ�ϵ�ص��CuSO4��Һ��FeCl3��FeCl2���Һ��ʾ��ͼ��ͼ1��ʾ������A��B��D��Ϊʯī�缫��CΪͭ�缫������һ��ʱ��Ͽ�K����ʱA��B�����ϲ��������������ͬ��
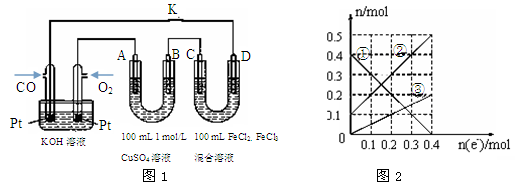
������A�������������ڱ�״���µ����Ϊ________________��
�ڱ�װ����Һ�н��������ӵ����ʵ�����ת�Ƶ��ӵ����ʵ����仯��ϵ��ͼ2��ʾ����ͼ�Т��߱�ʾ����________�������ӷ��ţ��ı仯����Ӧ������Ҫʹ��װ���н���������ǡ����ȫ��������Ҫ________ mL 5.0 mol��L��1 NaOH��Һ��
�ο��𰸣���1��C(s) + 2H2O(g) = CO2(g) + 2
���������
�����Ѷȣ�����
4������� ��һ��������ܱ������У��������»�ѧ��Ӧ��
  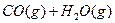 ���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±��� ���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±���
T/��
| 700
| 800
| 830
| 1000
| 1200
| K
| 0.6
| 0.9
| 1.0
| 1.7
| 2.6
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK= ��
��2���÷�ӦΪ ������ȡ����ȡ�����Ӧ��
��3�����жϸ÷�Ӧ�Ѵﵽ��ѧƽ��״̬�������ǣ� ��
A��������ѹǿ����
B�����������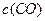 ���� ����
C��
D��
��4��ij�¶��£�ƽ��Ũ�ȷ�����ʽ�� �����жϴ�ʱ���¶�Ϊ �档 �����жϴ�ʱ���¶�Ϊ �档
�ο��𰸣���1�� ����������� �����������
�����Ѷȣ�һ��
5��ѡ���� ���ڷ�Ӧ: 2SO2(g)+O2(g)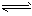 2SO3(g) �����ж���ȷ����[???? ] 2SO3(g) �����ж���ȷ����[???? ]
A��2���SO2������O2��Ӧ,�ض�����2���SO3
B��������������,����ѹǿ,ƽ�������ƶ�
C��ƽ��ʱ, SO2�������ʱض�����O2���������ʵ�����
D��ƽ��ʱ, SO2Ũ�ȱض�����O2Ũ�ȵ�����
�ο��𰸣�BC
���������
�����Ѷȣ�һ��
|
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772