��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪���淴ӦaA��bB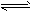 cC�У����ʵĺ���A����C�����¶ȵı仯������ͼ��ʾ������˵����ȷ����
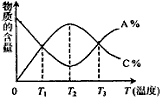
cC�У����ʵĺ���A����C�����¶ȵı仯������ͼ��ʾ������˵����ȷ����
 [???? ]
[???? ]
A���÷�Ӧ��T1��T3�¶�ʱ�ﵽ����ѧƽ��
B���÷�Ӧ��T2�¶�ʱ�ﵽ����ѧƽ��
C���÷�Ӧ������Ӧ�����ȷ�Ӧ
D�������¶ȣ�ƽ���������Ӧ�����ƶ�
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2������� �����ж�����Ӧ����Fe��s��+CO2��g���TFeO��s��+CO��g����ƽ�ⳣ��ΪK1��
��Fe��s��+H2O��g���TFeO��s��+H2��g����ƽ�ⳣ��ΪK2������ڲ�ͬ�¶��£�K1��K2ֵ���£�
| �¶�/�� | K1 | K2
500
1.00
3.15
700
1.50
2.25
900
2.50
1.50
��1����500��ʱ���з�Ӧ�٣�CO2��ʼŨ��Ϊ2mol/L��CO2��ת����Ϊ______��
��2����һ�����Ϊ10L���ܱ������У�����������Fe��FeO��ĩ��Ȼ��
���ٳ���CO2��H2O��g����1mol������һ�����¶ȣ����϶�����Ӧͬʱ�ﵽƽ�⣮��______��c(CO)
c(H2)
��ֵ���
���ٳ���CO22mol��H2?4mol��������900�棬���϶�����Ӧ�ﵽƽ�����ƽ��ʱ�������������______��
�ο��𰸣���1����CO2��Ũ�ȱ仯��Ϊcmol/L���ɷ���ʽ��֪CO��
���������
�����Ѷȣ�һ��
3��ѡ���� ������ʵ������������ԭ�����͵���
A��ʹ�ô��������ڼӿ�ϳɰ���Ӧ�ķ�Ӧ����
B�����Ṥҵ�У�������������������¯��
C��500�����ұ�������ʱ����������ߺϳɰ���ת����
D�������Ȼ�����Һʱ�����Ȼ������������У�Ȼ���ˮϡ��
�ο��𰸣�D
���������
�����������������ԭ��Ҳ����ƽ���ƶ�ԭ�������ô�ԭ�����͵���ʵ�߱������ص㣺�漰���淴Ӧ��ƽ���ƶ��ҷ���ƽ���ƶ�ԭ����A��ʹ�ô��������ڼӿ�ϳɰ���Ӧ�ķ�Ӧ���ʣ���ƽ�ⲻ�ƶ�����������������ԭ�����ͣ�����B�����Ṥҵ�У�������������������¯�У������˷�Ӧ��ĽӴ��������Ӧ���ʼӿ죬��ƽ�ⲻ�ƶ�����������������ԭ�����ͣ�����C���ϳɰ��ķ�ӦΪ���ȷ�Ӧ�����£�ƽ�������ƶ�������ת���ʽ��ͣ���������������ԭ�����ͣ�����D�������Ȼ�����Һʱ�����Ȼ������������У����������ӵ�ˮ�⣬������������ԭ�����ͣ���ȷ��
���㣺������������ԭ����Ӧ�á�
�����Ѷȣ�һ��
4������� ú��������úΪԭ�ϣ�������ѧ�ӹ�ʹúת��Ϊ���塢Һ�塢����ȼ���Լ����ֻ�����Ʒ�Ĺ�ҵ���̡�
(1)��ˮ����ͨ�����ȵ�̼���ɲ���ˮú������ӦΪ�� C(s)+H2O(g)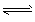 CO(g)+H2 (g) ��H =+131. 3kJ��mol-1 һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����____������ĸ����ͬ���� CO(g)+H2 (g) ��H =+131. 3kJ��mol-1 һ���¶��£���һ���ݻ��ɱ���ܱ������У�����������Ӧ���������жϸ÷�Ӧ�ﵽ��ѧƽ��״̬����____������ĸ����ͬ����
A�������е�ѹǿ����
B��1mol H-H�����ѵ�ͬʱ����2mol H-O��
C��v��(CO) =v��(H2O)
D��c(CO) =c(H2)
�ڸ��¶��£��÷�Ӧ��ƽ�ⳣ������ʽΪK=____��
(2)����ͬ����CO(g)��H2O(g)�ֱ�ͨ�뵽���Ϊ2L�ĺ����ܱ������У����з�Ӧ
CO(g)+H2O(g)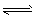 CO2 (g)+H2 (g)���õ������������ݣ� CO2 (g)+H2 (g)���õ������������ݣ�
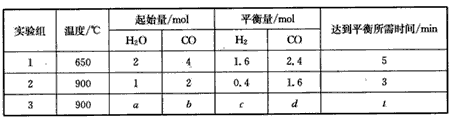
��ʵ��1����v(CO2)��ʾ�ķ�Ӧ����Ϊ____��
�ڸ÷�ӦΪ____��������š����ȷ�Ӧ��
����ʵ��3Ҫ�ﵽ��ʵ��2��ͬ��ƽ��״̬���������ʵ����������ֱ���ȣ�����t<3min����a��bӦ����Ĺ�ϵ��___���ú�a��b����ѧʽ��ʾ����
(3)Ŀǰ��ҵ����һ�ַ�������CO2�������״���һ�������·�����Ӧ��CO2(g)+ 3H2 (g) CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й�������������λΪ kJ��mol-1���ı仯�������Ϊ1L�ĺ����ܱ������У�����1mol CO2��3mol H2�����д�ʩ����ʹc(CH3OH)������� (? ?) CH3OH(g)+H2O(g)����ͼ��ʾ�÷�Ӧ���й�������������λΪ kJ��mol-1���ı仯�������Ϊ1L�ĺ����ܱ������У�����1mol CO2��3mol H2�����д�ʩ����ʹc(CH3OH)������� (? ?)
A�������¶�
B������He(g)��ʹ��ϵѹǿ����
C����H2O(g)����ϵ�з������
D���ٳ���1mol CO2��3mol H2

�ο��𰸣�(1)B��C��![]() ��������� ���������
�����Ѷȣ�һ��
5��ѡ���� һ�������£������Ϊ10L���ܱ������У�1 molX��1 molY������Ӧ��2x��g��+Y��g�� Z��g������60s�ﵽƽ�⣬����0��3mol Z������˵����ȷ���� Z��g������60s�ﵽƽ�⣬����0��3mol Z������˵����ȷ����
A����Ӧ����30 sʱ������Ӧ���ʵ����淴Ӧ����
B����Ӧ����80 sʱ���淴Ӧ���ʴ�������Ӧ����
C����Ӧ����60 sʱ��X�����ʵ���Ũ��Ϊ0��04 mol/L
D����Ӧ����60 sʱ��Y��ת����Ϊ70��
�ο��𰸣�C
���������
���������A�����ڷ�Ӧ��60s�ﵽƽ�⣬�����ڷ�Ӧ����30 sʱ������Ӧ���ʴ����淴Ӧ���ʣ�����B�����ڷ�Ӧ��60s�ﵽƽ�⣬��Ӧ����80 sʱ�������������ȱ仯����ƽ�Ᵽ�֣��淴Ӧ���ʵ�������Ӧ���ʣ�����C����Ӧ����60 sʱ������0��3mol Z �����ݷ�Ӧ����ʽ�и�������֮��Ĺ�ϵ����֪��X����0��6mol������0��4mol��X����X�����ʵ���Ũ��Ϊ0��4mol ��10L=0��04 mol/L����ȷ��D����Ӧ����60 sʱ���ﵽƽ�⣬���ݷ���ʽ��Y��Z�Ĺ�ϵ��֪��Ӧ����Z�����ʵ�����0��3mol����Y��ת����Ϊ(0��3mol ��1mol)��100%=30����
���㣺������淴Ӧ�еĻ�ѧ��Ӧ���ʺͻ�ѧƽ�⡢���ʵ�ת���ʵ�֪ʶ��
�����Ѷȣ�һ��
|
|