?
��1�����������У����Ʊ����̿�������ѡ����ʵ�����������ʵ�ֵ���?????????????�����������ƣ���ͬ�����ӷ�Ӧԭ���������Բ�ͬ�����������������???????????????��
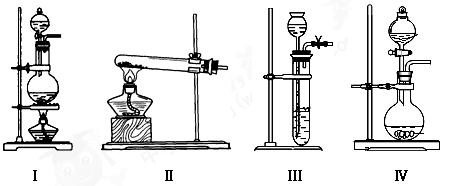
��2�����ݱ�������ʵ��ԭ����������װ����ѡ����ʵ����巢��װ�ã������ �������ϱ��еĿո��С� �������ϱ��еĿո��С�
��3��ijѧϰС�����������ͼʵ�飬����������ͨ������װ������֤���������ʣ�
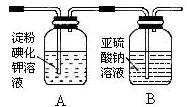 ? ?
��ͨ��������A�е�������??????????������ʵ��װ�ô��ڵ�����ȱ����??????????��
��������С��ͬѧ���һ��ʵ�飬֤��ϴ��ƿB�е�Na2SO3�ѱ�������
?????????????????????????????????????????????????????
��4�������ſ������ռ�Cl2�����±߷����ڻ��������ռ�װ��ͼ��?

��5�����������Cl2��100 mL 1.7mol/L��NaOH��Һ��ȫ���ա������պ����Һ���з������飬��֪��pH����13 �������Ƿ�Ӧǰ����Һ������仯����ClO����ClO3�������ʵ���Ũ��֮��Ϊ5��1���������������б����������������ʵ���Ϊ ??????????mol�� ??????????mol��
�ο��𰸣���13�֣�?��1��Cl2��1�֣��� NH3?��1�֣�
�����������
�����Ѷȣ�һ��
2��ʵ���� ��ͼΪ���������Ʊ������롢�����������֤�IJ�������װ��(�����豸���г̶ֹ�װ�þ���ȥ����֪�Ҵ��ķе�Ϊ78��5��)�������Ҫ������������� (����װ�ÿ�����ѡ�ã���Ҫʱ���ظ�ѡ��a��bΪ��ť)��
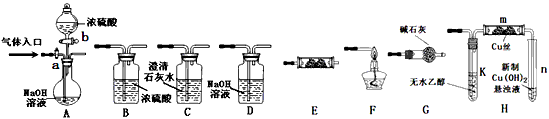
��1������A���������ͨ��CO��CO2�Ļ�����壬E�ڷ���CuO�����õ����������CO������֤�仹ԭ�Լ����������ѡװ�õ�����˳��ΪA��____��____��E��____��F (��дװ�ô���)��
������֤CO���������ʵ��������_____________________��
��2�����ʵ��ź�A����ťa�رգ�����E�ڷ���Na2O2����A��E��D��B��Hװ��˳����ȡ���������O2������O2�������Ҵ���
��Ϊ����������ر���ťa����������еIJ�����_____________________��
��Ϊ�õ�ƽ�ȵ��Ҵ�����������߷�ӦЧ�ʣ��ɲ�ȡ�Ĵ�ʩ�ǣ������ּ�����____________________��
m�з�����Ӧ�Ļ�ѧ����ʽ��____________________��
�ο��𰸣���1����C��B��C����AB֮���Cװ������Һ���ֳ��壬EF֮
���������
�����Ѷȣ�һ��
3��ʵ���� ��75�����ң�ʵ������HgSO4����������ʹ��Ȳ��ˮ��Ӧ��ȡ��ȩ��װ��ͼ���£����г�װ�þ�����ȥ��
��ѡ���Լ�����ʯ������CaS�����ʣ���HgO��ĩ��ŨH2SO4��NaOH��Һ������ˮ
������ʾ��CaS��ˮ�����H2S���壻HgSO4����H2S�ᷢ�������ж���ʧȥ���ԡ�
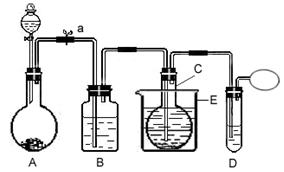
�ش��������⣺
��1������ҩƷǰ�������װ�ý��еIJ����ǣ�?????????????????????????????????��
��2��װ��B��ʢ�ŵ��Լ�Ϊ????????��?��������??��������������???????????
��3��д��A�з�������Ҫ��Ӧ�Ļ�ѧ����ʽ???????????????????????????????????
��4����Ӧ�¶�Ӧ������75�����ң�����Eװ�õ��ŵ���?????????????????????????
�ο��𰸣�
 ����������� �����������
�����Ѷȣ���
4��ʵ���� ��10�֣�ij��ȤС��ͬѧ��ͬ�������ͼ��ʾ��ʵ��װ�á���װ�üȿ�������ȡ���壬�ֿ�������֤���ʵ����ʡ�
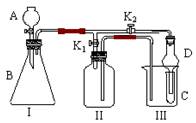
�Ŵ�K1�ر�K2������ȡijЩ���塣
��ͬѧ��Ϊװ��I��������ȡH2��NH3��O2����װ��IIֻ���ռ�H2��NH3�������ռ�O2����������???????��
��ͬѧ��Ϊ�ڲ��Ķ�װ��II������ǰ���£���װ��II�����ʵ��Ľ���Ҳ���ռ�O2������Ϊ���ĸĽ�������??????????????????????????????????????????????????��
�ƴ�K2�ر�K1���ܱȽ�һЩ���ʵ����ʡ�
��ͬѧ���ʵ��Ƚ������ԣ�KMnO4��Cl2��Br2����A�м�Ũ�����һ��ʱ�䣬�۲쵽C�е�������???????????????������D�ڸ�װ���е�������???????????????????????��
��ͬѧ��ʯ��ʯ�����ᡢ�����Ƶ�ҩƷ�������һʵ�顣����ʵ��Ŀ����???????????????????��
�ο��𰸣�(1)�������ܶȱȿ�����2�֣�?��װ��II��װ�Mˮ (2��
�����������
�����Ѷȣ���
5��ʵ���� 3λͬѧ���������3��ʵ�鷽������֤ij��ɫ�����мȺ���SO2���ֺ���CO2��
����1������ɫ����ͨ������KMnO4��Һ��KMnO4��Һ��ɫ����Ӧ������ͨ��ʯ��ˮ��ʯ��ˮ����ǡ�����֤ԭ��ɫ�����к���SO2���ֺ���CO2��
����2������ɫ����ͨ����ˮ����ˮ��ɫ��Ӧ������ͨ��ʯ��ˮ��ʯ��ˮ����ǣ�֤��ԭ��ɫ�����мȺ��� SO2���ֺ���CO2��
����3������ɫ����ͨ��Ʒ����Һ��������ͨ���ữKMnO4��Һ��Ʒ����Һ�����ͨ������ʯ��ˮ�����Ʒ����Һ��ɫ��KMnO4��Һ��ɫ��dzƷ����Һ����ɫ��ʯ��ˮ����ǣ�֤��ԭ��ɫ����Ⱥ���SO2���ֺ���CO2��
�Իش�����3�������У���֤��ԭ��ɫ�����м���SO2������CO2�ķ�������???????????????������������???????????????????��
�ο��𰸣���������ʵ������Ӧ�Ƿ���3������SO2���ڡ���SO2��֤��
�������������ʱһҪ����SO2��CO2�Ĺ����Ǿ���ʹ����ʯ��ˮ��룬��Ҫ���ǵ����ߵ�����SO2���л�ԭ�ԣ�����ʹƷ����ɫ��CO2���߱���Щ���ʡ���Ҫ������ʹ����KMnO4��Һ����ˮ��ɫ�����ʲ�����SO2������H2S��C2H4��C2H2�ȡ����֤������SO2����CO2��ʵ�����һ��ӦΪ������SO2���ڡ���SO2��֤��SO2�����ڡ�֤��CO2���ڡ�
�����Ѷȣ���
|