微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 用质量为100g 的铜作电极电解AgNO3溶液,电解一段时间后,两极的质量相差28g,此时两极质量分别是:阳极________________ ,阴极________________
参考答案:93.6g;121.6g
本题解析:
本题难度:一般
2、选择题 用石墨作电极电解2 mol・L-1NaCl和1 mol・L-1MgSO4混合溶液时,下列曲线合理的是
[??? ]
A.
B.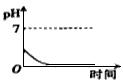
C.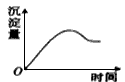
D.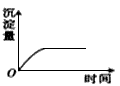
参考答案:D
本题解析:
本题难度:一般
3、选择题 下列各组的电极材料和电解质溶液中,不能组成原电池的是
A.铜片,石墨棒,稀硫酸
B.铜片,石墨棒,硝酸银溶液
C.锌片,铜片,稀盐酸
D.铜片,银片,FeCl3溶液
参考答案:A
本题解析:
试题分析:活泼性不同的电极,导线相连且插入电解质溶液中,才能构成原电池,据此可知选项BCD均可以构成原电池,A中铜与稀硫酸不反应,不能构成原电池,答案选A。
点评:该题是基础性试题的考查,试题难易适中,侧重对原电池原理和构成的考查。有助于培养学生的逻辑推理能力,提高学生的应试能力和学习效率。
本题难度:简单
4、推断题 镍电池广泛应用于混合动力汽车系统,电极材料由Ni(OH)2、炭粉、氧化铁等涂覆在铝箔上制成.由于电池使用后电极材料对环境有危害,某兴趣小组对该电池电极材料进行资源回收研究,并设计出相关实验流程图
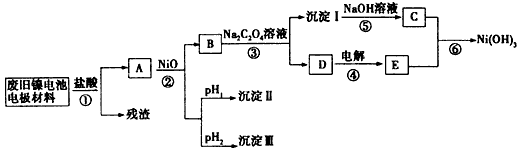
已知:①NiCl2易溶于水,Fe3+不能氧化Ni2+
②某温度下一些金属氢氧化物的Ksp及沉淀析出的理论pH如表所示:

回答下列问题:
(1)根据表数据判断步骤②依次析出沉淀Ⅱ 和沉淀Ⅲ (填化学式),则pH1 pH2(填填“>”、“=”或“<”),控制两种沉淀析出可利用 。
A.pH试纸 B.石蕊指示剂 C.pH计
(2)已知溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,则反应③的化学方程式是 。第③步反应后,过滤沉淀时需要的玻璃仪器有 。若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因 、 。
(3)④中阳极反应产生的气体E为 ,验证该气体的试剂为 。
(4)试写出反应⑥的离子方程式 。
参考答案:(1)Fe(OH)3 A
本题解析:由题给条件,金属氢氧化物的Ksp及沉淀析出的理论pH,可知,在A溶液中加入NiO是为了调节溶液pH,使相应的铝离子、三价铁离子全部沉淀出,Ni2+在溶液B中.根据pH可以确定开始析出沉淀和全部沉淀的pH范围,先析出沉淀Ⅱ是Fe(OH)3,沉淀pH范围是2.53~2.94,然后析出沉淀Ⅲ是Al(OH)3,沉淀PH的范围3.43~4.19,所以pH1<pH2;控制两种沉淀析出必须准确测定pH值,所以应利用pH计测定。
(2)由溶解度:NiC2O4>NiC2O4?H2O>NiC2O4?2H2O,结合流程中的变化
可知沉淀为溶解度小的NiC2O4?2H2O,所以根据转化关系写出化学方程式;
在过滤装置中用到的玻璃仪器和注意问题,根据装置和操作步骤写出NiCl2+Na2C2O4+2H2O=NiC2O4・2H2O+2NaCl,漏斗,烧杯、玻璃棒;滤纸破损、过滤液的液面高于滤纸的边缘。
(3)由流程图和以上分析可知,D溶液主要是氯化钠溶液,电解氯化钠溶液在阳极得到氯气,阴极得到氢气,所以E气体是Clc 2,验证氯气的试剂应是淀粉碘化钾溶液,遇氯气变蓝;
(4)在B溶液中加入Na2C2O4溶液生成了沉淀ⅠNiC2O4.2H2O,沉淀中加入氢氧化钠溶液,根据Ni(OH)2开始沉淀到全部沉淀的pH范围为7.60~9.75,加入过量氢氧化钠溶液能使沉淀NiC2O4・2H2O转化为Ni(OH)2,所以C为沉淀Ni(OH)2;根据流程图中的转化关系,沉淀C和氯气能生成Ni(OH)3,镍元素化合价升高是被氯气氧化的结果,因此离子方程式为2Ni(OH)2+2OH-+Cl2=2Ni(OH)3+2Cl-
本题难度:困难
5、选择题 能够实现反应Cu+2H2O===Cu(OH)2↓+H2↑的是[???? ]
A.铜银合金在潮湿空气中发生电化学腐蚀
B.用铜片作阴极、石墨作阳极,电解饱和氯化钠溶液
C.用铜片作阳极、石墨作阴极,电解饱和氯化钠溶液
D.铜片作原电池的负极,石墨作原电池的正极,氯化钠溶液作电解质溶液
参考答案:C
本题解析:
本题难度:一般