微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 (11分)下图为实验室制取、检验和收集纯净干燥的氯气的实验装置图:
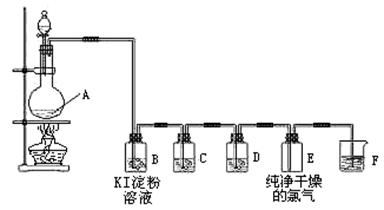
(1)装置A的化学方程式为:4HCl(浓)+MnO2 ?MnCl2+C12↑+2H2O,在方程式上标出电子转移的方向和数目;该反应的氧化剂是??????????;
?MnCl2+C12↑+2H2O,在方程式上标出电子转移的方向和数目;该反应的氧化剂是??????????;
(2)装置B中的现象是?????,反应的化学方程式为??????????????????????????。
(3)装置C中所装试剂是饱和食盐水,作用是除去??????????;装置D中所装试剂是????????,作用是???????????????。
(4)装置F是氯气的尾气处理装置,发生反应的离子方程式???????????????。
2、选择题 用氨水、盐酸、氢氧化钠中的任何一种溶液能鉴别的溶液组是(??)
①AgNO3和Al(NO3)3???②Na2CO3和BaCl2????③FeCl3和Fe2(SO4)3?????④NH4HCO3和MgCl2
A.只有①
B.只有④
C.①和④都能
D.全部都能
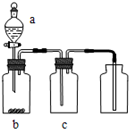
3、选择题 用图装置制取、提纯并收集表中的四种气体(a、b、c表示相应仪器中加入的试剂),其中可行的是( )
A.气体是NO2;a为浓硝酸;b为铜片;c为NaOH溶液
B.气体是SO2;a为浓硫酸;b为Cu;c为酸性品红溶液
C.气体是NH3;a为浓氨水;b为生石灰;c为浓硫酸
D.气体是CO2;a为稀盐酸;b为CaCO3;c为饱和NaHCO3溶液
4、选择题 下图是化学实验常用装置之一,若气体从右管进入,可用来收集的气体是
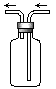 [???? ]
[???? ]
A. NO???????????
B.?NO2??????
C.?H2???????
D. CH4
5、填空题 (12分)过氧化钙晶体[CaO2・8H2O]较稳定,呈白色,微溶于水,能溶于酸性溶液。广泛应用于环境杀菌、消毒等领域。
Ⅰ.过氧化钙晶体的制备
工业上生产CaO2・8H2O的主要流程如下:
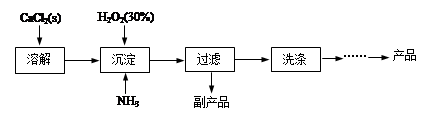

(1)用上述方法制取CaO2・8H2O的化学方程式是???????????????????。
(2)沉淀时常用冰水控制温度在10℃以下,其可能原因分别是???????????????????。
Ⅱ.过氧化钙晶体含量的测定
准确称取0.3000g产品于锥形瓶中,加入30 mL蒸馏水和10 mL 2.000 mol・L-1 H2SO4,用0.0200 mol・L―1KMnO4标准溶液滴定至终点。重复上述操作两次。H2O2和KMnO4反应的离子方程式为2MnO4-+5 H2O2+6H+ =2Mn2++5O2↑+8H2O
(3)滴定终点观察到的现象为??????????。
(4)根据表1数据,计算产品中CaO2・8H2O的质量分数(写出计算过程)
滴定次数
| 样品的质量/g
| KMnO4溶液的体积/mL
|
滴定前刻度/mL
| 滴定后刻度/mL
|
1
| 0.3000
| 1.02
| 24.04
|
2
| 0.3000
| 2.00
| 25.03
|
3
| 0.3000
| 0.20
| 23.24
???????????????????????????????????
|