微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 试用简单的实验证明,在醋酸溶液中存在着CH3COO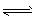 HCH3COO-+H+的电离平衡(要求写出简单操作、现象及实验能说明的问题)。
HCH3COO-+H+的电离平衡(要求写出简单操作、现象及实验能说明的问题)。
参考答案:在醋酸溶液中滴入紫色的石蕊试液,溶液呈红色,再向上述溶液中加
本题解析:
本题难度:一般
2、实验题 为确定HCl、H2CO3、H2SiO3的酸性强弱,某同学设计了如图所示的装置,一次实验即可达到目的(不必选其他酸性物质)。请据此回答
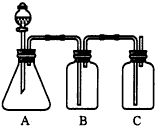
(1)锥形瓶中装某可溶性正盐溶液,分液漏斗所盛试剂应为_______________。
(2)装置B所盛的试剂是___________,其作用是________________。
(3)装置C所盛试剂是____________,C中反应的离子方程式是___________________。
参考答案:(1)盐酸
(2)饱和NaHCO3溶液;除去挥发出的
本题解析:
本题难度:一般
3、实验题 铁碳合金是以铁和碳为组元的二元合金,某化学学习小组设计了如图装置进行探究:
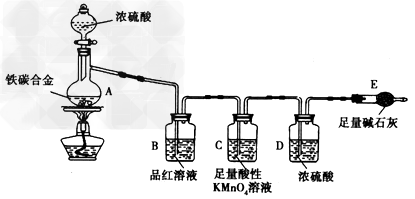
Ⅰ.浓硫酸的某些性质的定性探究:
(1)A中铁与浓硫酸发生反应的化学方程式是____________________。
(2)往A中滴加足量的浓硫酸,未点燃酒精灯前,观察A、B中的现象为________________________。
Ⅱ.铁碳合金中铁的定量探究:
(3)检查上述装置气密性的一种方法是:关闭分液漏斗的活塞,在E装置后面连上一根导管,然后____________,则证明装置的气密性良好。
(4)装置C的作用是______________________________________________________。
(5)称量E的质量,并蒋ag铁碳合金样品放入装置A中,再加入足量的浓硫酸,待A中不再逸出气体时,停止加热,拆下E并称重,E增重bg。铁碳合金中铁的质量分数为_________________________________。
(6)甲同学认为,依据此实验测得的数据计算合金中铁的质量分数可能会偏低,原因是空气中的CO2、H2O进入E 中使b增大。改进的方法是______________________________________________。
(7)乙同学认为,甲同学改进实验方法后,依据此实验测得的合金中铁的质量分数可能会偏高。你认为其中的原因是____________________________________________________________________________。
参考答案:(1)2Fe+6H2SO4(浓)![]() 本题解析:
本题解析:
本题难度:一般
4、实验题 某研究性学习小组在探究铝表面氧化膜对铝的保护时,设计了如下实验:
(1)取一小块铝片和一块锌片放入稀H2SO4中,看到锌片与酸反应产生H2速率很快,而铝片刚开始时,几乎看不到有气体,一段时间后,才看到有气体放出,随后产生气体速度逐渐加快,试解释其原因
_________________________________________。
(2)将铝片放入NaOH溶液,待看到有气体产生,取出铝片,用水洗涤,其作用是________________,该反应的化学方程式是________________________________。
(3)洗涤后的铝片放入Hg(NO3)2溶液,反应片刻。反应的化学方程式是__________________________。
(4)取出铝片用滤纸吸干后,在空气中很快就看到铝片上慢慢生成白色毛状物质,经分析该物质为氧化铝。写出反应的化学方程式____________________________,解释生成白色毛状物质的原因__________________________________________。
参考答案:(1)铝比锌活泼,反应速率应大于锌与酸反应速率,而该实验中刚
本题解析:
本题难度:一般
5、实验题 下图是用干燥纯净的Cl2与Cu粉反应来制取无水氯化铜的装置图,请回答下列问题:

⑴ 小试管的作用是????;烧瓶中发生反应的化学方程式是??????????????????????;
⑵ B瓶中的溶液是????????,其作用是??????????????????;C瓶中盛放的溶液是?????????,其作用是??????????????。
⑶ 玻璃管D中反应的现象是?????????????????。
⑷ 干燥管E中盛有碱石灰,其作用是?????????????????????????????????????。
⑸ 开始实验时,应先点燃??????处(填“A”或“D” )的酒精灯,当???????????时再点燃另一处的酒精灯。
参考答案:
 本题解析:略
本题解析:略
本题难度:简单