微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 一密闭容器中充人1mol N2和3mol H2,在一定条件下发生反应N2+3H2 2NH3,下列有关说法正确的是(??)
2NH3,下列有关说法正确的是(??)
A.达到化学平衡时,正反应和逆反应的速率都为零
B.当符合3u正(N2)=u正(H2)时,反应达到平衡状态
C.达到化学平衡时,单位时间消耗amolN2,同时生成3amolH2
D.当N2、H2、NH3的分子数比为1∶3∶2,反应达到平衡状态
参考答案:C
本题解析:
试题分析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以选项A不正确;选项B中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此B中的关系始终是成立,不正确;C中反应速率的方向相反,且满足反应速率之比是相应的化学计量数之比,正确;平衡时各种物质的浓度不再发生变化,但各种的浓度之间不一定满足某种关系,D不正确,答案选C。
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点、特征,然后结合具体的可逆反应灵活运用即可。
本题难度:一般
2、选择题 恒温下,将16?mol?N2与24?mol?H2的混合气体通入一个固定容积为4L的密闭容器中,发生如下反应:N2(g)+3H2(g) 2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说法正确的是?????[???? ]
2NH3(g),10分钟后反应达平衡时,NH3的含量(体积分数)为25%,下列的关说法正确的是?????[???? ]
A.达到平衡时,N2和H2的转化率之比为1:1 ??
B.10分钟内v(H2)=0.35mol/(L・min) ??
C.平衡混合气体的密度为128g/L ??
D.平衡混合气体中,n(N2):n(H2):n(NH3)=1:3:2
参考答案:C
本题解析:
本题难度:一般
3、填空题 (16分)氨的合成原理为:N2(g)+3H2(g) 2NH3(g) ;△H=" ―92.4" KJ・mol―1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题:
2NH3(g) ;△H=" ―92.4" KJ・mol―1。现在500℃、20 MPa时,将N2、H2置于一个容积为2 L的密闭容器中发生反应,反应过程中各物质的物质的量变化如下图。回答下列问题:
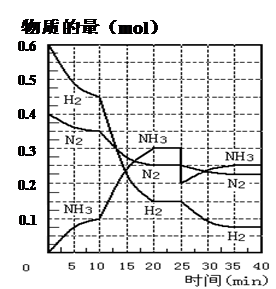
(1)10 min内以NH3表示的平均反应速率?????;
(2)在10 ~20 min内:NH3浓度变化的原因可能是 ??????;
A.加了催化剂
B.缩小容器体积
C.降低温度
D.增加NH3物质的量
(3)第1次平衡的时间范围为:???????,第2次平衡的时间范围为:?????,第1次平衡:平衡常数K1 = ?????(带数据的表达式),第2次平衡时NH3的体积分数 ??????????;
(4)在反应进行至25 min时:① 曲线发生变化的原因:??????② 达第二次平衡时,新平衡的平衡常数K2?????K1(填“大于”、“等于”、“小于”)
参考答案:⑴0.005 mol/(L.min)???⑵AB
⑶2
本题解析:
试题分析:(1)根据图像可知,10min时氨气的物质的量是0.1mol,浓度是0.05mol/L,所以其反应速率是0.05mol/L÷10min=0.005 mol・L-1 ・min-1。
(2)根据图像可知,在10 ~20 min内氨气的生成速率增大,再20min时反应达到平衡状态,所以改变的条件应该是使用了催化剂会缩小了容器容积,答案选AB。
(3)反应进行到25min是物质的浓度又方式变化,所以第1次平衡的时间范围为20~25 min;同样根据图像可知,第2次平衡的时间范围为35~40 min;第1次平衡时氨气、氮气和氢气的浓度分别是(mol/L)0.15、0.125和0.075,所以K =(0.15)2 /0.125×(0.075)3;第2次平衡时氨气、氮气和氢气的物质的量分别是(mol)0.25、0.225、0.075,所以氨气的体积分数是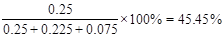 。
。
(4)①根据图像可知,25min是氨气的物质的量降低到0.2mol,而氮气和氢气的物质的量逐渐减小,所以改变的条件是移走0.1 mol NH3。②温度不变,所以平衡常数是不变的。
点评:本题综合性强,是高考的热点习题,主要考查学生的分析能力和思维能力。
本题难度:一般
4、选择题 在二氧化碳的水溶液中存在着如下平衡:
C02(g) C02(aq)??????????????????????? C02(aq)+H20
C02(aq)??????????????????????? C02(aq)+H20 H2C03(aq)
H2C03(aq)
H2C03(aq) H+ (aq)+HCO3-(aq)??????????? HCO3-(aq)
H+ (aq)+HCO3-(aq)??????????? HCO3-(aq)  H+(aq)+CO32-(aq)
H+(aq)+CO32-(aq)
下列有关说法正确的是(????)
A.水中溶解的二氧化碳的浓度,夏天时比冬天时高
B.如果海水略呈碱性,海水中二氧化碳的浓度比纯水高
C.气压升高,水中c(HCO3-)增大
D.常温下,二氧化碳的水溶液中,由水电离出的c(H+)与c(OH-)的乘积等于1×lO-14
参考答案:C
本题解析:略
本题难度:简单
5、选择题 C+CO2 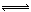 2CO(正反应吸热),反应速率为v1:N2+3H2?
2CO(正反应吸热),反应速率为v1:N2+3H2?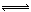 ?2NH3(正反应放热),反应速率为v2。对于上述反应,当温度降低时,v1和v2的变化情况是??????????(???)
?2NH3(正反应放热),反应速率为v2。对于上述反应,当温度降低时,v1和v2的变化情况是??????????(???)
A.同时增大
B.同时减小
C.v1增加,v2减小
D.v1减小,v2增大
参考答案:B
本题解析:对于任何反应,降低温度,化学反应速率减慢,与放热反应还是吸热反应无关;所以正确选项为B。
本题难度:简单