��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����������ȷ����
A����ⱥ��ʳ��ˮ���ռ�ʱ��Fe��������ʯī������
B������Ȼ�ͭʱ�������ϲ���������������������������ͭ���������
C�������ڿ����з����绯��ʴʱ����������
D��ԭ��ع���ʱ�������������صĸ���
�ο��𰸣�C
�����������ⱥ��ʳ��ˮ���ռ�ʱ��Fe��������ʴ��A������Ȼ�ͭʱ��������������ʧ������ȡ������ڿ����з����绯��ʴʱ������������ԭ��ع���ʱ�������������ص�������
�����Ѷȣ�һ��
2������� ��16�֣�2006����������ӵ���ܲ�������25��ֻ��﮵���������Բ��������Ľ�����Դ���������൱��ģ������������Դ��Ϊ��Ҫ���⡣ij�о�С���ij�Ͼ�����ӵ����������(ͼ�м�Ʒ��ϣ��ɷ�ΪLiMn2O4��ʯī�ۺ�����)���л����о��������������£�

��֪��Li2SO4��LiOH��Li2CO3��303K�µ��ܽ�ȷֱ�Ϊ34.2g��12.7g��1.3g��
��1����������NaOH��Һ��ȡ֮ǰ��Ҫ���з����������Ŀ����??????????????��
��2���Ͼɵ�ؿ������ڷŵ粻��ȫ��������﮵��ʣ�Ϊ�˰�ȫ�Բ�����Ҫ��______?__??????????????????��
��3��д����Ӧ�����ɳ���X�����ӷ���ʽ��
???????????????????????????????????????????��
��4����֪LiMn2O4��Mn�Ļ��ϼ�Ϊ+3��+4�ۣ�д����Ӧ�ڵ����ӷ�Ӧ����ʽ��
???????????????????????????????????????????��
��5������Li2CO3�Ļ�ѧ��Ӧ����ʽΪ______????????????????????????????__����֪Li2CO3��ˮ�е��ܽ�������¶����߶���С�����һ������ʱӦ_?????????_��
�ο��𰸣���1������Ӵ�������ӿ췴Ӧ���ʣ�2�֣�
��2��������
�����������1�����з��������������Ӧ��ĽӴ�������ӿ췴Ӧ���ʡ�
��2����ǻ��õĽ���������ˮ��������Ӧ��������Ҫ����������ˮ�֡�
��3����Һ�к���ƫ�����ƣ�����ͨ��CO2������������������������ʽΪCO2+AlO2�C+2H2O=Al(OH)3��+HCO3�C��
��4��LiMn2O4��Mn�Ļ��ϼ�Ϊ+3��+4�ۣ���+3�۵ı��������ɶ������̣�����ʽΪ4 LiMn2O4+4 H++O2=8MnO2+4 Li++2H2O��
��5��Li2CO3���ܽ��С������﮵ģ��������﮺�̼���Ʒ�Ӧ������
�����Ѷȣ�һ��
3��ѡ���� Ϊ�����ѧ���Ĺ�����ʶ��ij����ί�ٰ���һ�οƼ���������Ϊũ����Ǧ���صĽ���ʱ�����з�������ʧ����ǣ���֪Ǧ���صķ�ӦΪPb��PbO2��2H2SO4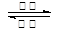 2PbSO4��2H2O����??��
2PbSO4��2H2O����??��
A��Ǧ��������������õĿɳ���أ��ڳ��ʱ����ص�����Ӧ��ֱ����Դ������
B��Ǧ�����ڷŵ�ʱ�����Һ�����Լ���
C��Ǧ�����ڷŵ�ʱ��PbO2��Ϊ����������ת��ΪPbSO4
D��Ǧ�����ڳ��ʱ��PbO2����������
�ο��𰸣�C
����������绯ѧ����ѧ��ѧ�е�һ����Ҫ֪ʶ�㣬ԭ��ء������ǻ�ѧ��������ת������Ҫװ�ã��������ǽ�������������һ���װ�á�ͨ��������Ӧ��Ԫ�ػ��ϼ۵ı仯������������ԭ��Ӧ�Ĺ��ɣ��Ǹ߿����ȵ㡣
�����ܷ�Ӧʽ�л��ϼ۵��������жϳ��������ŵ�ʱPbΪ������PbO2Ϊ������C������ʱ����������PbO2ΪPbSO4���������ӦΪ��������ֱ����Դ��������A�D����ȷ��Ǧ�����ڷŵ�ʱ������Ũ�Ȳ��ϱ�С�����Һ�����Լ�����B����ȷ����ΪC��
�����Ѷȣ�һ��
4��ѡ���� ���������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ���ܳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ3Zn��2K2FeO4��8H2O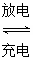 3Zn(OH)2��2Fe(OH)3��4KOH�����ڸõ�ص�˵����ȷ����(����)
3Zn(OH)2��2Fe(OH)3��4KOH�����ڸõ�ص�˵����ȷ����(����)
A���ŵ�ʱ��Zn��������������ԭ��Ӧ
B���ŵ�ʱ��K2FeO4������ҺpH��С
C�����ʱ��п��������ҺpH��С
D�����ʱ�������缫��ӦΪ��
Fe(OH)3��3e����5OH��=FeO ��4H2O
��4H2O
�ο��𰸣�D
����������ŵ�ʱ��Zn������������������Ӧ��������ӦΪ��FeO ��3e����4H2O=Fe(OH)3��5OH������ҺpH�����ʱ��п����ӦΪZn(OH)2��2e��=Zn��2OH������ҺpH����
��3e����4H2O=Fe(OH)3��5OH������ҺpH�����ʱ��п����ӦΪZn(OH)2��2e��=Zn��2OH������ҺpH����
�����Ѷȣ�һ��
5��ѡ���� ���������������������������
A�������ں�ˮ��
B��������ֲ������
C�����ڸ���Ŀ�����
D������������ˮ��
�ο��𰸣�A
������������������ں�ˮ�У�������ԭ��أ���ԭ����ܼӿ췴Ӧ���ʣ������������⣻
�����Ѷȣ���