��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� һ���¶��£���һ�������ı������ˮϡ�����У���Һ�ĵ��������仯����ͼ��ʾ������˵����ȷ����
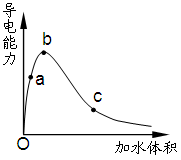
A��a��b��c������Һ��pH��c��a��b
B��a��b��c�������ĵ���̶ȣ�a��b��c
C����ʪ���pH��ֽ����a����Һ��pH���������ƫС
D��a��b��c������Һ��1mol/L����������Һ�кͣ���������������Һ�����c��a��b
�ο��𰸣�BC
���������������Һ�ĵ���������֪��������Ũ���ɴ�С��˳����bac������pH�ɴ�С��˳����cab��A����ȷ��ϡ�ʹٽ����룬ѡ��B��ȷ��pH��ֽ���������ʪ�����൱��ϡ�ʹ��ᣬ����a������Һ��ϡ��������Ũ��������ģ�����pH���С��C��ȷ��������ϡ�����У���������ʵ����Dz���ģ��к��������Ƶ������Dz���ģ�D����ȷ����ѡBC��
�����Ѷȣ�һ��
2������� ��5�֣������£�������һԪ�ᣨHX��HY��HZ���ֱ��NaOH��Һ�������ϣ�ʵ���������£�
��
| c(һԪ��) /mol��L�C1
| c(NaOH) /mol��L�C1
| �����Һ��pH
|
HX
| 0.1
| 0.1
| pH = x
|
HY
| 0.1
| 0.1
| pH = 7
|
HZ
| 0.1
| 0.1
| pH = 9
��1��������������һ������ǿ�����???��
��2��HZ��NaOH������Ӧ�����ӷ���ʽΪ???��������Һ��pH����7��ԭ����???���û�ѧ�� ��ʽ��ʾ����
��3��HX��Ӧ��������Һ�У���ˮ���������c(OH-)=???mol��L-1�����������Ƕ�x ֵ���жϣ��� ����ȷ����???��
A��һ��=7?? B.����<7??? C. һ���R7??? D.һ��>7
�ο��𰸣���5�֣���1��HY?????
��2��HZ +OH- =
���������
�����������1�������ʵ����������������ƻ�ϣ���Һ�������ȡ�������ǿ����������ǿ�ᣬ����Һ�����ԣ����������ᣬ����Һ�ʼ��ԣ�����������������һ������ǿ�����HY��
��2����HZ���������ƻ��Һ��pH�ж�HZ�����ᣬ�������ӷ���ʽʱ���ܲ��������ʽ���������ӷ���ʽΪHZ +OH- ="=" H2O + Z-��������Һ��pH����7��ԭ������ΪZ-ˮ��ʹ��Һ�ʼ��ԣ�ˮ������ӷ���ʽΪH2O + Z- �����Ѷȣ�һ�� �����Ѷȣ�һ��
3��ѡ���� ��ѧ�г�����ͼ������ʾij�ֱ仯���̣����й���4��ͼ���˵����ȷ���ǣ�������
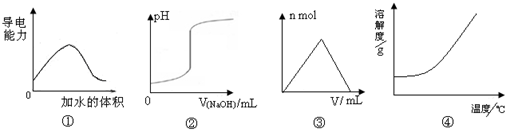
A��ͼ�ٿɱ�ʾt��ʱ��������ϡ��������Һ�����Եı仯
B��ͼ�ڿɱ�ʾ��һ���������еμ�һ��Ũ������������Һʱ����ҺpH�ı仯
C��ͼ�ۿɱ�ʾ��һ����������Һ�еμ�һ��Ũ������������Һʱ���������������ʵ����ı仯
D��ͼ�ܿɱ�ʾ���еĹ��������ܽ�����¶ȵı仯
�ο��𰸣�A����Һ������ǿ��ȡ������Һ������Ũ�ȵĴ�С�������Ĵ����
���������
�����Ѷȣ�һ��
4��ѡ���� �������Һ�����(��AG��ʾ)����Ϊc(H+)�� C(OH-)��ֵ�Ķ�������AG=lg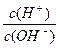 �������£����и���������AG��12����ɫ��Һ���ܴ����������(??? ) �������£����и���������AG��12����ɫ��Һ���ܴ����������(??? )
A��Mg2+��Ca2+��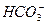 ��Cl- ��Cl-
B��K+��I-�� ��Br- ��Br-
C��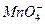 ��Ca2+��Cl-�� ��Ca2+��Cl-��
D��Na+��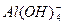 ��Cl-�� ��Cl-��
�ο��𰸣�B
�����������AG��12�����Ƴ���Һ��c(H+)��1��10-1 mol��L-1����Һ�����ԡ�ѡ��A��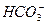 ������H+�������棻ѡ��C�� ������H+�������棻ѡ��C��
�����Ѷȣ���
5��ѡ���� 50��ʱ�����и���Һ�У����ӵ����ʵ���Ũ�ȹ�ϵ��ȷ����
A��pH=4�Ĵ����У�c(H+)=4.0mol?L��1
B������С�մ���Һ�У�c(Na+)= c(HCO3��)
C������ʳ��ˮ�У�c(Na+)+ c(H+)= c(Cl��)+c(OH��)
D��pH=12�Ĵ�����Һ�У�c(OH��)=1.0��10��2mol?L��1
�ο��𰸣�C
�������������Һ pH�������ʽ�ɵã�c(H+)=10��pHmol/L����pH=4�Ĵ�����c(H+)=10��4 mol?L��1��A�����С�մ�Ļ�ѧʽ��NaHCO3���������Ρ���ʽ�Σ���ˮ������ȫ���룬��NaHCO3="=" Na++HCO3���������Ӳ���ˮ�⣬��HCO3�������ٲ���ˮ������̼�ᣬ�����ٲ���HCO3�������̼������ӣ���HCO3��+H2O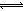 H2CO3+OH����HCO3�� H2CO3+OH����HCO3�� H++CO32��������ˮ��̶ȴ��ڵ���̶ȣ���С�մ���Һ�У�c(Na+)>c(HCO3��)��B�������ʳ��ˮ������ΪNaCl���ܼ�ΪH2O��ǰ��ȫ������ΪNa+��Cl�������߲��ֵ���ΪOH����H+�����ݵ���غ�ԭ���ɵã�c(Na+)+ c(H+)= c(Cl��)+c(OH��)��C����ȷ��25��ʱKw= c(H+)?c(OH��)=1.0��10��14��ˮ�ĵ��������ȷ�Ӧ�������¶��ܴ�ʹH2O H++CO32��������ˮ��̶ȴ��ڵ���̶ȣ���С�մ���Һ�У�c(Na+)>c(HCO3��)��B�������ʳ��ˮ������ΪNaCl���ܼ�ΪH2O��ǰ��ȫ������ΪNa+��Cl�������߲��ֵ���ΪOH����H+�����ݵ���غ�ԭ���ɵã�c(Na+)+ c(H+)= c(Cl��)+c(OH��)��C����ȷ��25��ʱKw= c(H+)?c(OH��)=1.0��10��14��ˮ�ĵ��������ȷ�Ӧ�������¶��ܴ�ʹH2O H++OH���ĵ���ƽ�����ƣ���50��ʱKw= c(H+)?c(OH��)>1.0��10��14��pH=12�Ĵ�����Һ��c(H+)=10��pHmol/L=10��12mol/L��c(OH��)= Kw/ c(H+)>1.0��10��2molL��1��D����� H++OH���ĵ���ƽ�����ƣ���50��ʱKw= c(H+)?c(OH��)>1.0��10��14��pH=12�Ĵ�����Һ��c(H+)=10��pHmol/L=10��12mol/L��c(OH��)= Kw/ c(H+)>1.0��10��2molL��1��D�����
��ѧ�������㶨λ�����⿼�鿼������ҺpH���˽⣻���鿼��������ˮ�⡢���������ˮ�еĵ�����˽⣻���鿼����ˮ��Һ������Ũ�ȴ�С�ıȽϣ����鿼����ˮ�ĵ���ƽ������ӻ��������˽⣻���鿼�����¶���ƽ�ⳣ����С��ϵ���˽⡣
��ѧ��������Ϊѧ������ʦѧ���������Ŷ�ԭ������Ȩѧ��������ʹ�ã����е��ã�������
����˫��ѡ���⣺�����2С�⣬ÿС��6�֣���12�֡���ÿС������ĸ�ѡ���У�������ѡ�������ĿҪ��ȫ��ѡ�Եĵ�6�֣�ֻѡ1������ȷ�ĵ�3�֣���ѡ����ĵ�0�֡�
�����Ѷȣ�һ��
|