微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
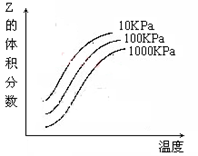
1、选择题 右图是温度和压强对X + Y  ?2Z 反应影响的示意图图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是(?????)。
?2Z 反应影响的示意图图中横坐标表示温度,纵坐标表示平衡混合气体中Z的体积分数。下列叙述正确的是(?????)。
A.上述可逆反应的正反应为放热反应
B.X、Y、Z均为气态
C.X和Y中只有一种是气态,Z为气态
D.上述反应的逆反应的△H>0
参考答案:C
本题解析:
试题分析:根据温度和压强对该反应影响的示意图可知,温度越高,Z的体积分数越大,说明正反应为吸热,△H>0,逆反应放热,△H<0,故A、D不正确;压强越大,Z的体积分数越小,说明反应平衡向逆向进行,根据勒夏特列定律,压强增大,平衡向体积减小的方向移动,说明反应物X和Y中只有一种是气态,生成物Z为气态,故B不正确,C正确,选C。
点评:本题考查化学平衡的知识,主要考查温度、压强对化学平衡的影响,题目难度不大,根据课本知识即可解答。
本题难度:简单
2、选择题 下列事实中,不能用勒沙特列原理解释的是(????)
A.开启啤酒瓶后,瓶中立刻泛起大量泡沫
B.在FeSO4溶液中加入少量铁粉以防止Fe2+被氧化
C.实验室中常用排饱和食盐水的方法收集Cl2
D.工业生产硫酸的过程中使用过量的空气以提高SO2的利用率
参考答案:B?
本题解析:勒沙特列原理适用于化学平衡。
本题难度:一般
3、选择题 对于反应2SO2(g)+O2 (g) 2SO3(g)(放热反应),下列判断正确的是
2SO3(g)(放热反应),下列判断正确的是
A.2体积SO2和足量O2反应,生成2体积SO3
B.其他条件不变,降低温度,正反应速率增大,逆反应速率减小
C.给定条件下该反应进行的限度为SO2消耗速率等于O2生成速率的两倍
D.平衡时,SO2浓度必定等于O2浓度的两倍
参考答案:C
本题解析:略
本题难度:一般
4、实验题 (11分)某研究性学习小组为证明2Fe3+ + 2I-  ?2Fe2+ + I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。
?2Fe2+ + I2为可逆反应(即反应存在一定的限度),设计如下几种方案。已知FeF63-是一种无色的稳定的络离子。
按要求回答下列问题。
方案甲:
取5mL 0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,再继续加入2mL CCl4,充分振荡。静置、分层,再取上层清液,滴加KSCN溶液。
(1)甲方案中能证明该反应为可逆反应的现象是????????????????????????????。
(2)有同学认为该方案设计不够严密,即使该反应为不可逆反应也可能出现上述现象,其原因是????????????????????????????????。
方案乙:
取5mL 0.1mol/L KI溶液,滴加2ml 0.1mol/L 的FeCl3溶液,溶液呈棕黄色,再往溶液中滴加NH4F溶液,若看到???????????????????现象,即可证明该反应为可逆反应,请解释产生该现象的原因???????????????????????????????????????。
方案丙:
设计如图原电池装置,接通灵敏电流计,指针向右偏转(注:灵敏电流计指针总是偏向电源正极),随着时间进行电流计读数逐渐变小,最后读数变为零。
当指针读数变零后,在乙烧杯中加入1mol/L FeCl2溶液,若观察到灵敏电流计的指针向?????方向偏转(填“左”、“右”或“不移动”),即可判断该反应为可逆反应,此时甲中石墨电极上的电极反应式为???????????????????????????。
参考答案:(1)下层(CCl4层)溶液呈紫红色,且上层清液中滴加KSC
本题解析:(1)根据实验数据可知碘化钾是过量的,若反应是可逆反应,则溶液中一定存在铁离子,同时也必须生成单质碘。所以可以通过检验铁离子和单质碘来证明。
(2)因为碘离子和亚铁离子在空气中也可以被氧气氧化生成单质碘和铁离子,所以方案不是很严密。
(3)可以依据外界条件对平衡的影响来验证。因为Fe3+与F-络合生成无色的FeF63-,促使2Fe3+ + 2I-  ?2Fe2+ + I2平衡朝逆反应方向移动,所以溶液颜色会变浅。
?2Fe2+ + I2平衡朝逆反应方向移动,所以溶液颜色会变浅。
(4)在原电池中负极是失去电子的,碘离子失去电子,所以电子是从甲池流向乙池,所以电流计的指针向左偏转。
本题难度:一般
5、填空题 在一固定容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g) 2NH3(g)?△H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
2NH3(g)?△H<0 。反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:

根据图,计算从反应开始到平衡时,平均反应速率v(NH3)=???????????。
⑵下列描述中能说明上述反应已达平衡的是?????。
A.3v正(H2)=2v逆(NH3)
B.容器中气体的平均相对分子量不随时间而变化
C.容器中气体的密度不随时间而变化
D.容器中气体的分子总数不随时间而变化
⑶ 第5分钟末,保持恒温恒压,若继续通入0.2mol的N2和0.6mol的H2,平衡????移动(填“向正反应方向”、“向逆反应方向”或“不”)。
参考答案:(1)0.025mol/(L・min)(2分,漏写单位扣1分
本题解析:
试题分析:(1)由图判断反应第4分钟时反应达到平衡,v(NH3)=0.1÷4=0.025mol/(L・min);(2)
A、不符合化学计量数关系,错误;B、容器中气体的平均相对分子量是一个不断变化的量,当不变时即达到平衡,正确;C、该容器体积不变,密度是一个恒量,错误;D、分子个数是一个变量,当不变时即达到平衡,正确。(3)改变条件后的平衡与原平衡好是等效平衡,故平衡不移动。
本题难度:一般