微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 用NA表示阿伏加德罗常数,下列说法中正确的是(??)???????????????????????
A.2.4 g金属镁与足量盐酸反应,转移电子的数目为0.1NA
B.1L 1 mol/L的CaCl2溶液中含Cl-的数目为NA
C.在25℃、1.01×105 Pa的条件下,2.24L H2中含有的分子数小于0.1NA
D.标准状况下11.2 L CCl4含有分子数为0.5NA
参考答案:C
本题解析:略
本题难度:一般
2、选择题 设nA为阿伏加德罗常数的数值,下列说法正确的是
A.常温下,18gH2O中含有2nA个氢原子
B.标准状况下,22.4L苯含有nA个苯分子
C.1mol Na与足量水反应转移2nA个电子
D.0.1 mol?L-1CH3COOH溶液中含有0.1nA个CH3COO-
参考答案:A
本题解析:
试题分析:水的相对分子质量为18,由于n=m/M,则n(H2O)=1mol,由于物质组成关系式H2O~2H中氢原子与水分子的系数之比等于物质的量之比,则n(H)="2" n(H2O)=2mol,故A选项正确;标准状况下苯是液体,不能用V/22.4L?mol―1求出其物质的量为1mol,故B选项错误;钠与水发生置换反应,生成NaOH和H2,钠元素由0价升为+1价,根据化合价升高总数等于转移电子数可得:2Na+2H2O=2NaOH+H2↑~2e―,其中转移电子与钠的系数之比等于物质的量之比,则2mol
本题难度:简单
3、选择题 0.5mol氢气在标准状况下所占的体积约是( )
A.22.4L
B.11.2L
C.5.6L
D.2.24L
参考答案:B
本题解析:标准状况下,气体的摩尔体积是22.4L/mol,所以根据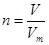 可知,0.5mol氢气在标准状况下所占的体积0.5mol×22.4L/mol=11.2L,答案选B。
可知,0.5mol氢气在标准状况下所占的体积0.5mol×22.4L/mol=11.2L,答案选B。
本题难度:一般
4、填空题 (4分)10.4gR2SO4中含0. 1molR2+,则R2SO4的摩尔质量是 ;R的相对原子质量是 。
参考答案:(4分)208g・mol-1(2分);
本题解析:略
本题难度:一般
5、实验题 某次实验需用0.4 mol/L NaOH溶液480 mL。配制方法如下:
(1)配制该溶液应选用_______________mL容量瓶;???
(2)用托盘天平准确称量__________g 固体NaOH;
(3)将称量好的NaOH固体放在500 mL大烧杯中,倒入约300 mL蒸馏水,用玻璃棒搅拌,使固体全部溶解,待__________________后,将烧杯中的溶液注入容量瓶中;用少量蒸馏水洗涤烧杯??????????次,洗涤后的溶液一并转入容量瓶,轻轻晃动容量瓶,使溶液混合均匀;向容量瓶中加入蒸馏水,到液面_____________________时,改用__________加蒸馏水至液面最低点与刻度线相切。盖好瓶塞,上下颠倒混合均 91EXAm.org匀;若在配制过程中出现下列情况,将使所配制的NaOH溶液的浓度偏高的是___________,偏低的是___________,对实验结果没有影响的是___________(填各选项的序号)。
A.所用的NaOH中混有少量Na2O
B.用托盘天平称量一定质量固体NaOH时,所用的小烧杯内壁不太干燥
C.配制溶液所用的容量瓶洗净后没有烘干
D.固体NaOH在烧杯中溶解后,立即将溶液转移到容量瓶内并接着进行后续操作
E.转移溶液后,未洗涤烧杯和玻璃棒就直接定容
F.最后确定NaOH溶液体积(定容)时,俯视观察液面与容量瓶刻度线
G.定容摇匀后静止,发现液面低于刻度线,再加蒸馏水至刻度线。
参考答案:(1)500
(2)8.0?
(3)待冷却至室温
本题解析:
试题分析:(1)因溶液的体积480mL,但容量瓶的规格没有480mL,所以选用500mL容量瓶,故答案为:500mL;
(2)需氢氧化钠的质量为m=0.5L×0.4mol?L-1×40g/mol=8.0g,故答案为:8.0;
(3)氢氧化钠溶解放出大量的热,溶液具有热胀冷缩的性质,影响溶液体积,故应先冷却至室温,故答案为:待溶液冷却至室温;
(4)为保证溶质尽可能转移到容量瓶中,需用少量蒸馏水洗涤烧杯2-3?次,并将洗涤液一起转入容量瓶中,故答案为:蒸馏水;一起转入容量瓶中;
本题难度:一般