微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 若以w1和w2分别表示物质的量浓度为a mol/L和b mol/L硫酸的质量分数,且知其2a=b,则下列推断正确的是
A.2ω1=ω2
B.ω1=2ω2
C.2ω1<ω2
D.ω1<ω2<2ω1
参考答案:C
本题解析:硫酸的质量分数越大,溶液的密度越大,设a mol/L的硫酸的密度为ρ1,b mol/L硫酸的密度为ρ2,则根据物质的量浓度与溶质质量分数的关系: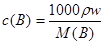 可得
可得
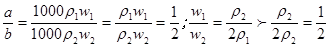 ,即得2ω1<ω2
,即得2ω1<ω2
本题难度:一般
2、选择题 下列数量的各物质所含原子个数按由大到小顺序排列的是( )
①0.75mol氨气;②4g氦气;③4℃时9ml水;④11.2L甲烷(标况)
A.①④③②
B.④③②①
C.②③④①
D.①④②③
参考答案:①氨气分子含有4个原子,原子的物质的量为氨气的4倍,0.75
本题解析:
本题难度:简单
3、选择题 使等体积的AlCl3.CaCl2.NaCl溶液中的Cl-完全转化为AgCl沉淀,所用0.1 mol/L AgNO3溶液的体积相同,则这三种溶液的物质的量浓度之比为( )
A.1:2:3
B.1:1:1
C.2:3:6
D.6:3:2
参考答案:C
本题解析:
试题分析:分别加入足量的硝酸银溶液,Cl-沉淀完全时,消耗等物质的量的AgNO3,可知AlCl3、CaCl2、NaCl三种溶液中含氯离子的物质的量相同,假设n(Cl-)=1mol,根据物质的化学式可知:n(NaCl)=1mol,n(CaCl2)=1/2mol,n(AlCl3)=1/3mol,溶液的体积相同,则物质的量之比等于物质的量浓度之比,所以,三种溶液的物质的量浓度之比为1/3:1/2:1=2:3:6,故C项正确。
考点:本题考查物质的量浓度的计算。
本题难度:一般
4、选择题 1 mol/L H2SO4的含义是
A.1L水中含有1mol H2SO4
B.1L溶液中含有1mol H+
C.1L H2SO4溶液中含98g H2SO4
D.将98g H2SO4溶于1L水配成溶液
参考答案:C
本题解析:单位体积溶液中溶质的溶质的物质的量是物质的量浓度,所以1 mol/L H2SO4的含义是1L H2SO4溶液中含1mol硫酸,即98g H2SO4,答案选C。
本题难度:简单
5、选择题 用NA表示阿伏加德罗常数的值,下列说法正确的是(?? )
A.1mol苯乙烯中含有的碳碳双键的数目为4NA
B.2.24L乙炔在空气中完全燃烧,生成0.2NA个CO2分子
C.1.7g羟基所含电子数目为NA
D.1.4g戊烯和聚丙烯的混合物中含碳原子的物质的量为0.1NA
参考答案:D
本题解析:
试题分析:注意苯环中不含碳碳双键,则苯乙烯中只含有一个碳碳双键,所以1mol苯乙烯中含有的碳碳双键的数目为NA ;由于没有注明是否为标准状况,所以不能换算;1.7g羟基为0.1mol,一个羟基中含有9个 电子,所以1.7g羟基所含电子数目为0.9NA;由于戊烯和聚丙烯中碳、氢的质量比相等,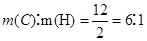 本题难度:一般
本题难度:一般