微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成。由蛇纹石制取碱式碳酸镁的实验步骤如图
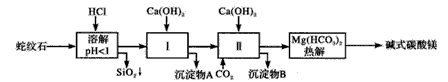
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是____。
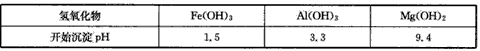
(2)进行I操作时,控制溶液pH=7~8(有关氢氧化物沉淀的pH见上表)Ca(OH)2不能过量,若Ca(OH)2过量可能会导致____溶解、____沉淀。
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入____(填人物质的化学式),然后 ____(依次填写实验操作名称)。
(4)物质循环使用,能节约资源。上述实验中,可以循环使用的物质是____(填写物质化学式)。
(5)现设计一个实验,确定产品aMgCO3・bMg(OH)2・cH2O中a、b、c的值,请完善下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量
②高温分解
③____
④____
⑤MgO称量
(6)18. 2g产品完全分解后,产生6.6gCO2和8.0gMgO,由此可知,产品的化学式中:
a=____;b=____;c=___
参考答案:(1)Fe3+、Al3+
(2)Al(OH)3 ;M
本题解析:
本题难度:一般
2、实验题 单晶硅是信息产业中重要的基础材料。通常用炭在高温下还原二氧化硅制得粗硅(含铁、铝、硼、磷等杂质),粗硅与氯气反应生成四氯化硅(反应温度450~500℃),四氯化硅经提纯后用氢气还原可得高纯硅。以下是实验室制备四氯化硅的装置示意图。
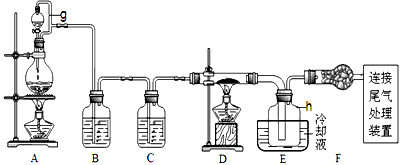
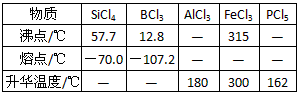
相关信息如下:①四氯化硅遇水极易水解; ②硼、铝、铁、磷在高温下均能与氯气直接反应生成相应的氯化物;③有关物质的物理常数见下表
请回答下列问题:
(1)写出装置A中发生反应的离子方程式____________________。
(2)装置A中g管的作用是____________________;装置C中的试剂是____________________;装置E中的h瓶需要冷却的理由是____________________。
(3)装置E中h瓶收集到的粗产物可通过精馏(类似多次蒸馏)得到高纯度四氯化硅,精馏后的残留物中,除铁元素外可能还含有的杂质元素是__________(填写元素符号)。
(4)为了分析残留物中铁元素的含量,先将残留物预处理,使铁元素还原成Fe2+,再用KMnO4标准溶液在酸性条件下进行氧化还原滴定,反应的离子方程式是:5Fe2++MnO4-+8H+==5Fe3++Mn2++4H2O
①滴定前是否要滴加指示剂?____(填“是”或“否”),请说明理由____________________。
②某同学称取5.000g残留物后,经预处理后在容量瓶中配制成100 mL溶液,移取25.00 mL试样溶液,用1.000×10-2 mol/L KMnO4标准溶液滴定。达到滴定终点时,消耗标准溶液20.00 mL,则残留物中铁元素的质量分数是_____________。
参考答案:(1)MnO2+4H++2Cl-![]() 本题解析:
本题解析:
本题难度:一般
3、实验题 草酸是一种重要的化工产品。实验室用硝酸氧化淀粉水解液制备草酸的装置如图所示(加热、搅拌和仪器固定装置均已略去)实验过程如下

① 将一定量的淀粉水解液加入三颈瓶中
② 控制反应液温度在55~60℃条件下,边搅拌边缓慢滴加一定量含有适量催化剂的混酸(65%HNO3与
98%H2SO4的质量比为2∶1.5)溶液
③ 反应3h左右,冷却,抽滤后再重结晶得草酸晶体。硝酸氧化淀粉水解液过程中可发生下列反应:
C6H12O6+12HNO3→3H2C2O4+9NO2↑ +3NO↑+9H2O
C6H12O6+8HNO3→6CO2↑+8NO↑ +10H2O
3H2C2O4+2HNO3 →6CO2↑+2NO↑ +4H2O
(1)检验淀粉是否水解完全所需用的试剂为_____________________。
(2)实验中若混酸滴加过快,将导致草酸产率下降,其原因是___________________。
(3)装置C用于尾气吸收,当尾气中n(NO2):n(NO)=1:1时,过量的NaOH溶液能将NO,全部吸收,原因是___________________(用化学方程式表示)。
(4)与用NaOH溶液吸收尾气相比较,若用淀粉水解液吸收尾气,其优、缺点是___________________。
(5)草酸重结晶的减压过滤操作中,除烧杯、玻璃棒外,还必须使用属于硅酸盐材料的仪器有
___________________。
参考答案:(1)碘水或KI-I2溶液
(2)由于温度过高、硝酸浓
本题解析:
本题难度:一般
4、实验题 (1)乙酸是生活中常见的有机物之一,乙酸的官能团为____________(写名称)。用食醋浸泡有水垢(主要成分是CaCO3)的暖瓶或水壶,可以清除其中的水垢。写出该反应的方程式:___________________。
在试管A中加入3mL乙醇,然后边振荡试管边慢慢加入2mL浓硫酸和2mL乙酸,按下图所示连接好装置进行实验,以制取乙酸乙酯。
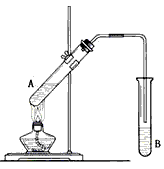
(2)试管B中盛放的溶液是_______________,其作用是:______________________
(3)乙醇与乙酸反应的化学方程式是:_______________________;反应类型________________
(4)实验完成后,试管B的液面上有透明的不溶于水的油状液体产生。若分离B中的液体混合物需要用到的玻璃仪器主要是___________________________。
参考答案:(1)羧基;2CH3COOH+CaCO3==(CH3COO)
本题解析:
本题难度:一般
5、实验题 CuSO4・5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4・5H2O的实验室制备流程图。
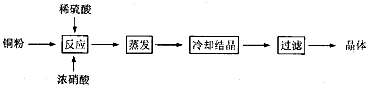
根据题意完成下列填空:
(1)向含铜粉的稀硫酸中滴加浓硝酸,在铜粉溶解时可以观察到的实验现象:______________________、________________________。
(2)如果铜粉、硫酸及硝酸都比较纯净,则制得的CuSO4・5H2O中可能存在的杂质是___________,除去这种杂质的实验操作称为____________________________。
(3)已知:CuSO4+2NaOH=Cu(OH)2↓+Na2SO4称取0.1000 g提纯后的CuSO4・5H2O试样于锥形瓶中,加入0.1000 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸20.16 mL,则0.1000 g该试样中含CuSO4・5H2O____________g。
(4)上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用___________。在滴定中,准确读数应该是滴定管上蓝线_______________________所对应的刻度。
(5)如果采用重量法测定CuSO4・5H2O的含量,完成下列步骤:①_______________②加水溶解③加氯化钡溶液,沉淀④过滤(其余步骤省略) 在过滤前,需要检验是否沉淀完全,其操作是__________________。
(6)如果1.040 g提纯后的试样中含CuSO4・5H2O的准确值为1.015 g,而实验测定结果是l.000 g 测定的相对误差为___________________。
参考答案:(1)溶液呈蓝色;有红棕色气体产生
(2)Cu(NO3
本题解析:
本题难度:一般