微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在100 mL某一元弱酸的溶 液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示。
液中,以0.50 mol/L氢氧化钠溶液滴定后得滴定曲线如图所示。
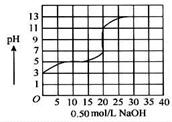
下列叙述正确的是( )
A.该弱酸在滴定前 的浓度是0.15 mol/L
的浓度是0.15 mol/L
B.该弱酸稀释10倍后pH为4
C.滴定过程为求滴定终点,最合适的指示剂是酚酞
D.滴定过程为求滴定终点,最合适的指示剂是甲基橙
参考答案:C
本题解析:略
本题难度:一般
2、选择题 下列物质能使紫色石蕊试液由紫变红又退色的是
①Cl2?②盐酸?③氯水?④盐酸酸化的漂白粉溶液?⑤木炭
A.①②③
B.①③④
C.②③④
D.①③④⑤
参考答案:B
本题解析:
正确答案:B
①Cl2③氯水?④盐酸酸化的漂白粉溶液三种物质遇到紫色石蕊试液先显酸性,由紫变红,后显强氧化性,漂白,红色褪去;②盐酸,只显酸性;⑤木炭具有吸附性。
本题难度:一般
3、选择题 完全燃烧一定质量的无水乙醇,放出的热量为Q,为完全吸收生成的CO2,并使之生成正盐Na2CO3,消耗掉0.8mol/L NaOH溶液500mL,则燃烧1mol酒精放出的热量是
A.0.2Q
B.0.1Q
C.5Q
D.10Q
参考答案:D
本题解析:CO2为0.8mol/L×0.5L÷2=0.2mol,C2H5OH为0.1mol,燃烧1mol酒精放出的热量是10Q,选D。
本题难度:一般
4、选择题 下列物质加入水中,能使水的电离程度增大,且所得溶液显酸性的是(???)
A.CH3COOH
B.Al2(SO4)3
C.NaOH
D.Na2CO3
参考答案:B
本题解析:影响水的电离平衡的外界条件有:温度、溶液酸碱性、盐类水解等。将CH3COOH加入水中,则增大水中的[H+],从而会抑制水的电离,减小了的电离程度,但是由于CH3COOH的电离,溶液呈酸性。NaOH的加入,则增大水中的[OH-],从而会抑制水的电离,减小了水的电离程度,溶液呈碱性。B、D都是盐类,并且一个是强酸弱碱盐,一个是强碱弱酸盐,把它们加入到水中,都会发生水解,结合水电离产生的OH-和H+,使平衡向电离的方向移动,从而会促进水的电离。
本题难度:简单
5、填空题 现有浓度均为0.1 mol/L的下列溶液:
①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵
请回答下列问题:
(1)①②③④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)________。
(2)将③和④等体积混合后,混合液中各离子浓度由大到小的顺序是____。
(3)已知T ℃,KW=1×10-13,则t ℃________(填“>”、“<”或“=”)25℃。在T℃时将pH=11的NaOH溶液a L与pH=1的H2SO4溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=________。
(4)25℃时,有pH=x的盐酸和pH=y的氢氧化钠溶液(x≤6,y≥8),取a L该盐酸与b L该氢氧化钠溶液反应,恰好完全中和,求:
①若x+y=14,则a/b=________(填数据);
②若x+y=13,则a/b=________(填数据);
③若x+y>14,则a/b=________(填表达式);
④该盐酸与该氢氧化钠溶液完全中和,两溶液的pH(x、y)的关系式为__(填表达式)。
参考答案:(1)④②③①
(2)c(Na+)=c(Cl-)>
本题解析:(1)向溶液中加入酸或碱均能抑制H2O的电离,且溶液中H+或OH-浓度越大,由水电离出的H+浓度越小;盐的水解能促进水的电离,即由水电离出c(H+)的从大到小的顺序为④②③①。(2)二者完全反应生成NaCl和NH3・H2O,NH3・H2O电离使溶液呈碱性,即c(Na+)=c(Cl-)>c(OH-)>c(NH4+)>c(H+)。(3)温度升高时KW增大,T℃时KW>1×10-14,即T℃>25℃;NaOH溶液中n(OH-)=0.01a mol,H2SO4中n(H+)=0.1bm
本题难度:一般