微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 碳酸钠俗称纯碱,其用途很广。实验室中,用碳酸氢铵和饱和食盐水可制得纯碱。各物质在不同温度下的溶解度见表。
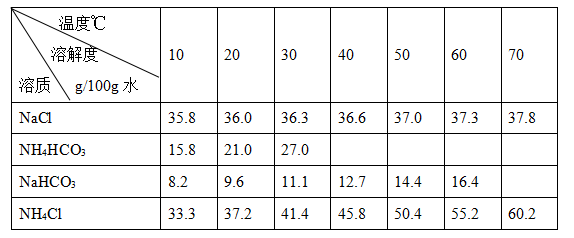
实验步骤
Ⅰ、化盐与精制:①粗盐(含Ca2+、Mg2+、SO42-)溶解;②加入足量NaOH和Na2CO3溶液,煮沸;③过滤;④加入盐酸调pH至7。
Ⅱ、转化:①将精制后的食盐溶液温度控制在30~35℃之间;在不断搅拌下,加入研细的碳酸氢铵;保温,搅拌半小时;②静置,a 、b ;③得到NaHCO3晶体。
Ⅲ、制纯碱:将得的NaHCO3放入蒸发皿中,在酒精灯上灼烧,冷却到室温,即得到纯碱。
完成下列填空:
(1)“化盐与精制”可除去的粗盐中的杂质离子是????????????????。
(2)“转化”的离子方程式是?????????????????????????????????。
(3)“转化”过程中,温度控制在30~35℃之间的加热方式是??????????????;为什么温度控制在30~35℃之间???????????????????????????????。
(4)a、b处的操作分别是????????????、????????????。
(5)实验室制得的纯碱含少量NaCl还可能含少量NaHCO3,为测定纯碱的纯度,用电子天平准确称取样品G克,将其放入锥形瓶中用适量蒸馏水溶解,滴加2滴酚酞,用c mol/L的标准盐酸滴定至溶液由浅红色变成无色且半分钟不变,滴定过程中无气体产生,所用盐酸的体积为V1mL。此时发生的反应为:
CO32-+H+→HCO3-
①样品中碳酸钠质量百分含量的表达式是??????????????。
②向锥形瓶溶液中继续滴加2滴甲基橙,用同浓度的盐酸继续滴定至终点,所用盐酸的体积为V2mL。滴定终点时溶液颜色的变化是?????????????;根据实验数据,如何判断样品含NaHCO3??????????????????。
参考答案:(1)Ca2+、Mg2+
(2)Na++HCO3-→N
本题解析:(1)足量NaOH可以除去Mg2+;Na2CO3可以除去Ca2+;
(2)Na++HCO3-→NaHCO3↓
(3)根据水浴加热,温度易控制且受热均匀;温度过高造成NH4HCO3分解,温度过低,NH4HCO3的溶解度小;
(4)NH4HCO3与NaCl反应生成NaHCO3,便有晶体析出,然后过滤、洗涤可得到NaHCO3。
(5)①酚酞做指示剂,用浓度为cmol/LHCl溶液滴定至溶液由红色变成无色,说明CO32-+H+→HCO3-反应达到终点,所用盐酸的体积为V1mL,则碳酸钠的质
本题难度:困难
2、选择题 在25℃,101Kpa下由HCHO (g)、H2和CO组成的混合气体共6.72 g,将该气体与2.24 L氧气(标准状况)充分反应后的产物通过足量的Na2O2粉末,使Na2O2粉末增重的质量为(???)
A.等于6.72 g
B.小于6.72 g
C.大于6.72 g
D.无法计算
参考答案:B
本题解析:由反应CO+Na2O2=Na2CO3;H2+Na2O2=2NaOH有混合气全部与过氧化钠结合,故增加的质量为6.72g。
本题难度:简单
3、选择题 下列有关钠的叙述正确的是
A.钠在空气中燃烧生成氧化钠
B.钠元素在自然界中可以以游离态形式存在
C.少量金属钠可以保存在煤油中
D.金属钠投入硫酸铜溶液中有铜生成
参考答案:C
本题解析:
试题分析:A、钠在空气中燃烧生成过氧化钠,错误;B、钠化学性质活泼,易与空气中的水、氧气反应,在自然界中只能以化合态存在,错误;C、少量金属钠可以保存在煤油中,正确;D、金属钠投入硫酸铜溶液中,钠先与水反应生成氢氧化钠和氢气,氢氧化铜再与硫酸铜溶液中反应生成氢氧化铜,错误。
本题难度:一般
4、填空题 (5分)标准状况下,向100mLNaOH溶液中慢慢通入CO2气体充分反应后,在所得溶液M中逐滴加入1mol/L盐酸,(反应前后溶液体积变化忽略不计)所得气体体积和所加盐酸的体积关系如图。

(1)c(NaOH)=???????
(2)取M溶液40mL与等体积的1mol/L盐酸按各种可能方式混合,产生气体的体积为VmL,则V的取值范围为??????????????。
参考答案:(1)3mol/L???(2)0≤V≤448mL
本题解析:略
本题难度:简单
5、计算题 在含有35.8g Na2CO3和NaHCO3混合物的溶液中加入200mL 某浓度的盐酸,恰好完全反应,生成8.96L CO2(标准状况)。问:
(1)原溶液中有??????????mol Na2CO3,??????????mol NaHCO3。
(2)盐酸的物质的量浓度。
参考答案:(1)Na2CO3:0.1 mol,NaHCO3:0.3 m
本题解析:略
本题难度:一般