微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (1)将该温度下a mL pH="13" NaOH溶液与b mL0.05mol/L H2SO4混合,所得混合溶液的pH=7,
则a:b =
(2)若在含有足量AgCl固体的饱和AgCl溶液中分别放入:
A.100mL蒸馏水中;
B.100mL 0.2 mol・L-1AgNO3溶液中;
C.100 mL 0.1 mol・L-1AlCl3溶液中;
D.100mL 0.1 mol・L-1盐酸溶液中。
充分搅拌后,银离子浓度最小的是 (填序号)
(3)在25℃下,向浓度均为0.20 mol・L-1的MgCl2和CuCl2混合溶液中逐滴加入氨水,先生成 沉淀(填化学式),生成该沉淀的离子方程式为 ;当测得溶液pH=11.00时,则此温度下残留在溶液中的c(Mg2+):c(Cu2+)=
(已知25℃时Ksp[Mg(OH)2]=1.8×10-11,KsP[Cu(OH)2]=2.0×10-20)
参考答案:(1) 1(2) C (3)  本题解析:
本题解析:
试题分析:(1)由题意可知氢离子浓度等于氢氧根离子浓度,而氢氧根离子浓度由离子离子积常数10-14除以10-13等于0.1故氢氧根离子的物质的量为0.1a 氢离子物质的量为0.05乘以2乘以b 等于0.1b所以a:b =1 (2)C选项会抑制AgCl的电离,且氯化铝中氯的浓度最大,所以答案选C。(3)由题目可知氢氧化铜的溶解平衡常数最小,所以先生成氢氧化铜 ,
考点:考查离子平衡移动及溶解平衡的相关知识
本题难度:一般
2、填空题 (1)pH=13的CH3COONa溶液加水稀释100倍后,pH 11(填“>”“=”或“<”),原因是 (用离子方程式和必要的文字说明);pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后CH3COONa溶液的pH NaOH溶液的pH(填“>”“=”或“<”);
(2)pH相等时,①NH4Cl ②(NH4)2SO4 ③NH4HSO4三种溶液中c(NH4+)由大到小的顺序为 ;
(3)等体积、等浓度的氢氧化钠与醋酸混合后溶液呈 性,溶液中c(Na+) c(CH3COO-)(填“>”“=”或“<”);pH=13的氢氧化钠与pH=1的醋酸等体积混合后溶液呈 性,溶液中c(Na+)
c(CH3COO-)(填“>”“=”或“<”);
(4)25℃,用0.1000 mol / LNaOH溶液滴定20.00mL0.1000mol/L某一元酸HA溶液所得滴定曲线如图。
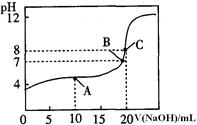
①为减小实验误差,由图可知滴定时指示剂应选用 (填“石蕊”、“酚酞”、“甲基橙”);
②A、B、C三点所示溶液导电能力最强的是 点对应的溶液;
③25OC,HA的电离平衡常数约为 。
参考答案:(1) > 加水稀释使平衡CH3COO-+H2O
本题解析:
试题分析:
(1)首先写出CH3COO-+H2O CH3COOH+OH-,加水稀释,假设平衡不移动,那么c(OH-)=10-1 mol・L-1÷100=10-3 mol・L-1,但平衡右移c(OH-)应比10-3 mol・L-1大,所以最终溶液中c(OH-)>10-3 mol・L-1;加热促进了CH3COO-的水解,使c(OH-)增大。
CH3COOH+OH-,加水稀释,假设平衡不移动,那么c(OH-)=10-1 mol・L-1÷100=10-3 mol・L-1,但平衡右移c(OH-)应比10-3 mol・L-1大,所以最终溶液中c(OH-)>10-3 mol・L-1;加热促进了CH3COO-的水解,使c(OH-)增大。
(2)依据NH4++H2O NH3・H2O+H+,因为①、②中的H+全部是水解生成的,且c(H+)相同,所以c(NH4+)①=②;由NH4HSO4=NH4++H++SO42-可知③中的H+大部分是电离生成的,所以c(NH4HSO4)远远小于c(NH4Cl)。
NH3・H2O+H+,因为①、②中的H+全部是水解生成的,且c(H+)相同,所以c(NH4+)①=②;由NH4HSO4=NH4++H++SO42-可知③中的H+大部分是电离生成的,所以c(NH4HSO4)远远小于c(NH4Cl)。
(3)正好完全中和生成CH3COONa,CH3COO-水解,显碱性;混合后溶液中含有CH3COONa、CH3COOH,显酸性,溶液中存在CH3COONa=CH3COO-+Na+、CH3COO-+H2O CH3COOH+OH-、CH3COOH
CH3COOH+OH-、CH3COOH CH3COO-+H+、H2O
CH3COO-+H+、H2O OH-+H+,CH3COOH的电离程度大于CH3COO-的水解程度,所以电离生成的CH3COO-大于水解消耗的CH3COO-,即c(Na+)<c(CH3COO-);我们也可以用电荷守恒c(OH-)+c(CH3COO-)=c(H+)+c(Na+)求解,因为混合后溶液呈酸性,所以c(H+)>c(OH-),所以c(Na+)<c(CH3COO-)。
OH-+H+,CH3COOH的电离程度大于CH3COO-的水解程度,所以电离生成的CH3COO-大于水解消耗的CH3COO-,即c(Na+)<c(CH3COO-);我们也可以用电荷守恒c(OH-)+c(CH3COO-)=c(H+)+c(Na+)求解,因为混合后溶液呈酸性,所以c(H+)>c(OH-),所以c(Na+)<c(CH3COO-)。
(4)①石蕊变色范围PH5.8――8.0 由红色变为蓝色,甲基橙变色范围 PH3.1――4.4 由红色变为黄色,酚酞变色范围 PH8.2――10.0 由无色变为红色,故选酚酞。
②C为强碱性溶液,离子浓度最大。
③C点,PH=8.则c(OH-)=10ˉ6 mol /L对于CH3COO-+H2O CH3COOH+OH-,c(OH-)=10ˉ6 mol/L,则c(CH3COOH)=10ˉ6 mol/L。c(CH3COO-)=20.00mL*0.1000mol/L/40mL=0.05mol/L。CH3COO-水解程度较小,可以忽略。所以该平衡的平衡常数为K1= c(OH-)* c(CH3COOH)/ c(CH3COO-)=2*10ˉ11。
CH3COOH+OH-,c(OH-)=10ˉ6 mol/L,则c(CH3COOH)=10ˉ6 mol/L。c(CH3COO-)=20.00mL*0.1000mol/L/40mL=0.05mol/L。CH3COO-水解程度较小,可以忽略。所以该平衡的平衡常数为K1= c(OH-)* c(CH3COOH)/ c(CH3COO-)=2*10ˉ11。
CH3COO-+H2O CH3COOH+OH- K1=2*10ˉ11
CH3COOH+OH- K1=2*10ˉ11
H2O H++OH- Kw=10ˉ14
H++OH- Kw=10ˉ14
CH3COOH CH3COO-+H+ K=?
CH3COO-+H+ K=?
解得:K=5×10ˉ4
考点:电解质溶液PH的计算,酸碱中和滴定
本题难度:困难
3、填空题 (9分)现有浓度均为0.1 mol/L的下列溶液:①硫酸 ②醋酸 ③氢氧化钠 ④氯化铵⑤硫酸铝 ⑥碳酸氢钠。请回答下列问题:
(1)①②③④四种溶液中由水电 离出的H+浓度由大到小的顺序是 (填序号)。
离出的H+浓度由大到小的顺序是 (填序号)。
(2)已知T℃,Kw = 1×10-13,则T℃ (填“>”、“<”、“=”)25℃。在T℃时,将pH = 11的③溶液a L与pH = 1的①溶液b L混合(忽略混合后溶液体积的变化),若所得溶液的pH = 10,则a:b = 。
(3)将⑤溶液和⑥溶液混合时,可看到的实验现象是 ,产生该现象的原因是 (用离子方程式解释原因)。
参考答案:(9分)
(1)④②③①(2分)
(2)>(1分
本题解析:略
本题难度:简单
4、选择题 下列图示与对应的叙述相符的是( )
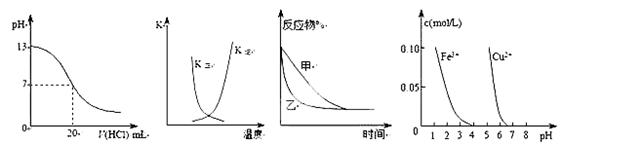
① ② ③ ④
A.图①表示25℃时,用0.1 mol・L-1盐酸滴定20 mL 0.1 mol・L-1NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2A(g) + B(g) 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化
2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化
C.图③表示压强对可逆反应2A(g)+2B(g)  3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
D.据图④若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右。
参考答案:D
本题解析:
试题分析:A.当加入盐酸20mL时,pH发生骤变,题中pH变化曲线不正确,如下图,A错误
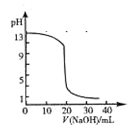
B.反应2A(g)+B(g) 2C(g)△H>0,温度升高反应正向进行,正反应速率大于逆反应速率,故B错误;C.2A(g)+2B(g)
2C(g)△H>0,温度升高反应正向进行,正反应速率大于逆反应速率,故B错误;C.2A(g)+2B(g) 3C(g)+D(s)反应是气体体积变化的反应,压强改变,平衡发生移动,故C错误;D.若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在3-4左右,铁离子沉淀完全,D正确;故选D.
3C(g)+D(s)反应是气体体积变化的反应,压强改变,平衡发生移动,故C错误;D.若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在3-4左右,铁离子沉淀完全,D正确;故选D.
考点:化学平衡常数的含义;体积百分含量随温度、压强变化曲线;难溶电解质的溶解平衡及沉淀转化的本质
本题难度:一般
5、选择题 下列措施能使水的电离程度增大的是
[?? ? ]
A.加入盐酸溶液
B.加醋酸钠????
C.?? 加入氨水????
D.???降温
参考答案:C
本题解析:
本题难度:简单