微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在同温同压下,某气体与氧气质量相同,体积之比为2:1,则该气体的式量为
A.64
B.44
C.28
D.16
参考答案:D
本题解析:分析:同温同压下,体积之比等于物质的量之比.所以质量相同的该气体与氧气的物质的量之比为2:1,令质量为mg,再根据n=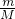 计算气体摩尔质量,摩尔质量以g/mol作单位,数值上等于该气体的相对分子质量.
计算气体摩尔质量,摩尔质量以g/mol作单位,数值上等于该气体的相对分子质量.
解答:同温同压下,体积之比等于物质的量之比.
所以质量相同的该气体与氧气的物质的量之比为2:1,
令质量为mg,则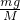 :
: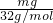 =2:1,
=2:1,
所以M=16g/mol,所以该气体的式量为16.
故选:D.
点评:考查阿伏伽德罗定律,难度中等,本题也可根据同温同压下,相同质量的气体,体积之比与摩尔质量成反比计算.
本题难度:一般
2、选择题 下列实验操作均要用玻璃棒,其中与过滤操作中玻璃棒的作用相同的是
A.测溶液pH
B.蒸发
C.溶解
D.向容量瓶转移液体
参考答案:D
本题解析:分析:玻璃棒在很多操作中被用到,不同操作中玻璃棒的作用也不相同,如引流、搅拌加速溶解、防止液体飞溅、转移固体等作用.
在过滤操作中的作用是引流;在蒸发操作和配制溶液中是搅拌;蒸发完毕可以用玻璃棒转移固体;玻璃棒还能起的作用是蘸取少许溶液测pH;红磷燃烧试验中引燃红磷; 在溶解固体时是用玻璃棒来加速溶解,在过滤中用玻璃棒是引导液体的流向,防止外流,据此即可解答.
解答:A.玻璃棒在测溶液pH时起蘸取少许溶液的作用,与过滤中用玻璃棒是引导液体的流向,防止外流不同,故A错误;
B.在蒸发实验中玻璃棒的作用是搅拌,防止液体因局部受热而飞溅,蒸发完毕可以用玻璃棒转移固体,与过滤中用玻璃棒是引导液体的流向,防止外流不同,故B错误;
C.玻璃棒的作用是搅拌,加速物质的溶解,与过滤中用玻璃棒是引导液体的流向,防止外流不同,故C错误;
D.向容量瓶转移液体时玻璃棒起引流作用,与过滤中用玻璃棒是引导液体的流向,防止外流相同,故D正确;
故选D.
点评:本题主要考查了玻璃棒的作用,熟悉各实验中玻璃棒的作用及使用注意事项即可解答,题目较简单.
本题难度:困难
3、选择题 化学工作者从反应RH+Cl2(g)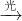 RCl(l)+HCl(g)受启发,提出在农药和有机合成工业中可获得副产品盐酸.这一设想已成为现实.试指出从上述反应产物中得到盐酸可能用到的最佳分离方法是
RCl(l)+HCl(g)受启发,提出在农药和有机合成工业中可获得副产品盐酸.这一设想已成为现实.试指出从上述反应产物中得到盐酸可能用到的最佳分离方法是
A.蒸馏法
B.水洗分液法
C.升华法
D.有机溶剂萃取法
参考答案:B
本题解析:分析:由反应RH+Cl2(g)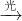 RCl(l)+HCl(g)可知,生成物为RCl和HCl,利用它们的溶解性来分析.
RCl(l)+HCl(g)可知,生成物为RCl和HCl,利用它们的溶解性来分析.
解答:因RCl不溶于水,而HCl易溶于水,可用水洗分液法分离,
故选B.
点评:本题考查学生物质分离的方法,熟记物质的性质是解题的关键所在,难度不大.
本题难度:简单
4、选择题 在标况下,下列气体含有的分子数最多的是
A.17g NH3
B.67.2L Cl2
C.4g H2
D.0.5mol SO2
参考答案:B
本题解析:分析:计算各物质的物质的量,根据N=nNA可知,物质的量越大,分子数目越多.通过比较物质的量判断.
解答:A、17g氨气的物质的量为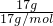 =1mol,
=1mol,
B、标准状况下,67.2L的氯气的物质的量为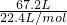 =3mol,
=3mol,
C、4g氢气的物质的量为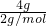 =2mol,
=2mol,
D、0.5mol SO2.
所以各物质的物质的量为B>C>A>D.
故选:B.
点评:考查常用化学计量的有关计算,难度不大,注意公式的运用与基础知识的掌握.
本题难度:一般
5、选择题 体积为V?mL,密度为ρ?g/mL的溶液,含有相对分子质量为M的溶质m?g,其物质的量浓度为c?mol/L,溶液的质量分数为W%,下列表示式中,不正确的是
A.c=
B.m=
C.W%=
D.c=
参考答案:A
本题解析:分析:溶液的质量为Vρ,溶质的质量为mg,可根据c= =
=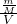 =
= 进行相关的计算.
进行相关的计算.
解答:A.c= =
=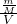 =
= mol/L=
mol/L= mol/L,故A错误;
mol/L,故A错误;
B.m=m(溶液)×W%=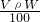 g,故B正确;
g,故B正确;
C.W%=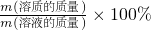 =
=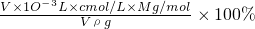 =
= ,故C正确;
,故C正确;
D.c= =
= =
= mol/L,故D正确.
mol/L,故D正确.
故选A.
点评:本题考查物质的量浓度的计算,侧重于物质的量的相关计算公式的综合运用,题目难度不大,注意把握相关计算公式.
本题难度:简单