微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 常温下,0.1 mol・L-1CH3COONa溶液pH =a,则下列说法正确的是
A.CH3COOH在常温下Ka数值约为l×101-2a
B.约有1.0×l0a-14 mol・L-1的水发生电离
C.加热后溶液pH <a
D.加少量水后,溶液pH >a
参考答案:B
本题解析:
试题分析:由水的离子积常数与水解平衡常数可计算出电离平衡常数,可判断A错;由于水解是一个吸热反应过程,故加热后水解平衡正向移动,氢氧根离子浓度增大,碱性增强,pH增大;加水稀释后溶液的浓度减小,故碱性减弱,pH减小。
考点:考查水解平衡的相关知识点
本题难度:一般
2、选择题 盐酸、醋酸和碳酸氢钠是生活中常见的物质。下列表述正确的是[???? ]
A.l0mL0.10mol/LCH3COOH溶液加入等物质的量的NaOH后,溶液中离子浓度由大到小的顺序是c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-)
C.在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO32-和OH-
D.中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH的物质的量相同
参考答案:A
本题解析:
本题难度:一般
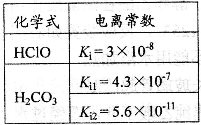
3、选择题 根据右表提供的数据,判断在等浓度的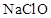 、
、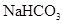 混合溶液中,各种离子浓度关系正确的是 ( )
混合溶液中,各种离子浓度关系正确的是 ( )
A.
B.
C.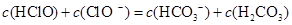
D.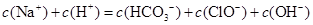
参考答案:A
本题解析:
试题分析:由电离常数可知电离关系为:H2CO3>HClO>HCO3-,则同浓度时水解程度为:CO32->ClO->HCO3-。由于同浓度时,ClO-水解程度大于HCO3-,A项正确,B项不正确。由物料守恒c(HClO)+c(ClO-)=c(HCO3-)+c(H2CO3)+c(CO32-)知,C项不正确。由电荷守恒c(Na+)+c(H+)=c(HCO3-)+c(ClO-)+c(OH-)+2c(CO32-)知,D项不正确。答案选A。
考点:水解平衡
点评:本题主要根据电荷守恒和物料守恒以及越弱越水解来进行判断,本题难度较大,考查学生的分析能力。
本题难度:困难
4、填空题 (1)将等质量的锌粉分别投入10 mL 1 mol/L HCl和10 mL 1 mol/L的CH3COOH溶液中,产生H2的体积分别为V1和V2;①若锌不足量,反应速率快的是_______?????? ___;②若锌过量,产生H2的量有何关系__________。
(2)将等质量的锌粉分别投入c(H+)均为1 mol/L体积均为10 mL的盐酸和醋酸溶液中,产生H2的体积分别为V1和V2;①若锌不足量,反应速率快的是_______????? ___;②若锌过量,产生H2的量有何关系__________。
参考答案:(1)①锌粒与盐酸反应?????②V1=V2
(2)①
本题解析:(1)①盐酸是强酸,而醋酸是燃烧,再浓度相等的条件下,盐酸的反应速率快。
②由于两种酸的物质的量是相同的,因此生成的氢气是相同的。
(2)由于是醋酸是弱酸,所以在氢离子浓度相等的条件下,醋酸的浓度大,因此醋酸的反应速率快。由于醋酸的浓度大,因此生成的氢气多。
本题难度:一般
5、选择题 PH=3的盐酸和醋酸各100mL,分别和锌反应,反应完后,放出的气体一样多。若最后有一溶液中锌剩余,则下列判断正确的是 ( )
A.反应开始时速率v(HCl)> v(CH3COOH)
B.加入的锌质量相等
C.盐酸中锌有剩余
D.反应开始后不久,醋酸反应的速率小于盐酸
参考答案:C
本题解析:略
本题难度:一般