��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����ԭ��ؾ���������ʽϸߣ�ѭ�����������ŵ㡣�乤��ԭ���ɱ�ʾΪ��2Na+xS Na2Sx���������¶ȹ��������ָ����ܵ�ص�ȱ�ݣ���ѧ���о����֣����ö����
Na2Sx���������¶ȹ��������ָ����ܵ�ص�ȱ�ݣ���ѧ���о����֣����ö����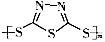 ����Ϊ�缫��Ӧ���ϣ�����Ч�ؽ��͵�صĹ����¶ȣ���ԭ���ϼ������Ͷ����������オ���ԡ������й�������ȷ����
����Ϊ�缫��Ӧ���ϣ�����Ч�ؽ��͵�صĹ����¶ȣ���ԭ���ϼ������Ͷ����������オ���ԡ������й�������ȷ����
A�������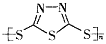 ����һ���������ǽ�������
����һ���������ǽ�������
B������� �������ﲻ�ܷ����ӳɷ�Ӧ
�������ﲻ�ܷ����ӳɷ�Ӧ
C��ԭ��صĸ�����Ӧ�ǽ�����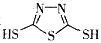 ת��Ϊ
ת��Ϊ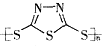 �Ĺ���
����
D������·����0.02mol����ͨ��ʱ��ԭ��صĸ���������ԭ��0.46g
�ο��𰸣�D
���������
���������Aѡ���������һ�־ۺ�����ڸ߷��Ӳ��ϣ���A����Bѡ��˶������к��в����ͼ����ܷ����ӳɷ�Ӧ����B����Cѡ����ݵ�ط�Ӧ��֪ԭ��صĸ����ǽ����Ʒ���ʧ���ӵ�������Ӧ����C����Dѡ����ݵ缫��Ӧʽ��ÿ����2 mol�Ľ����ƣ�����ת��2 mol������·��ת��0.02 mol����ʱ��������ԭ��صĸ�����Ӧԭ��0.46 g����D��ȷ����ѡD��
�����Ѷȣ�һ��
2��ѡ���� ������������ȷ���ǣ�������
A���ò��缫���NaOH��Һ��һ��ʱ�����Һ�����ʵ�������������
B���õ�ⷨ������ͭʱ����ͭ������
C���ö��Ե缫���100mL����ʳ��ˮ������112mL�����������ʱ������������Ũ��ԼΪ0.05mol/L���ٶ���Һ�����Ϊ100mL��
D��ͭпԭ��ع���ʱ�����������·�õ�����
�ο��𰸣�A���ò��缫���NaOH��Һʱ������������������ʧ����������
���������
�����Ѷȣ���
3��ѡ���� һ����ѧ��ص��ܷ�Ӧ����ʽΪ��Zn+Cu2+==Zn2++Cu���û�ѧ��ص���ɿ���Ϊ ( )
A B C D
���� Cu Cu Zn Fe
���� Zn Zn Cu Zn
�������Һ H2SO4 CuSO4 ZnCl2 CuCl2
�ο��𰸣�BD
�����������
�����Ѷȣ�һ��
4��ѡ���� ��1��ijԭ��ص��ܷ�Ӧ�����ӷ���ʽ�ǣ�Zn+Cu2+==Zn2++Cu���˷�Ӧ��ԭ��ص���ȷ����� [???? ]
����
����
�������Һ
A��
Cu
Zn
HCl
B��
Zn
Cu
CuSO4
C��
Cu
Zn
CuSO4
D��
Cu
Zn
ZnCl2
��2��������ͼԭ���װ�õ���������ȷ����
 [???? ]
[???? ]
A��ͭ��������ͭƬ�������ݲ���
B��ͭƬ��������
C��������пƬ����������ͭƬ
D����������ͭƬ���汻��ԭ
�ο��𰸣���1��C
��2��D
���������
�����Ѷȣ���
5������� ��4�֣����켼��ʹ��������ؾ��и��ܡ���㣬����Ⱦ�ŵ㣬����ȼ�ϵ������ʽ�ͼ�ʽ���֣����Ƿŵ�ʱ�ĵ���ܷ�Ӧʽ���ɱ�ʾΪ��2H2��O2 ="==" 2H2O ��
��ʽ����ȼ�ϵ�صĵ��������:
�为����ӦΪ��2H2��4e��="==" 4H������������ӦΪ????????????????????����
��ʽ����ȼ�ϵ�صĵ�����Ǽ
��������Ӧ��ʾΪ��O2��2H2O��4e��= 4OH��������ӦΪ��????????????????????????��
�ο��𰸣�����4�֣�ÿ��2�֣���
������O2+ 4H�� + 4e
���������
������ʱ����2H2��O2 ="==" 2H2O��ȥ2H2��4e��="==" 4H������������Ӧ��O2+ 4H�� + 4e- ="=" 2H2O������ʱ����2H2��O2 ="==" 2H2O��ȥO2��2H2O��4e��= 4OH�����ø�����Ӧ2H2 + 4OH�D �C 4e- ="=" 4H2O��
��֮������ԭ��صĵ缫ʽ����д��ֻҪ֪���ܷ�Ӧʽ������Ӧ����ʽ�����Ϊ����ʽ��
�����Ѷȣ�һ��