微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述正确的是
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2 mol?L-1的盐酸,与等体积水混合后pH=1
D.pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7
2、填空题 (6分)现有浓度均为0.1 mol/L的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸铵、⑦硫酸氢铵,⑧氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)??????。
(2)④、⑤、⑥、⑦、⑧五种溶液中NH4+浓度由大到小的顺序是(填序号)???????
(3)将②和③等体积混合后,混合液中各离子浓度由大到小的顺序是
(4)已知t℃,KW=1×10-13,则t℃(填“>”或“<”或“=”) ??25℃。在t℃时将pH=11的NaOH溶液a L与pH=1的H2SO4的溶液b L混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=2,则a∶b= ??。
(5)若室温时pH=a的氨水与pH=b的盐酸等体积混合,恰好完全反应,则该氨水的电离度可表示为 ?????????
3、计算题 有一pH为12的NaOH溶液100mL,如果将其pH降为11,那么,
(1)若用蒸馏水应加入______mL;
(2)若用pH=10的NaOH溶液应加入______mL;
(3)若用pH=2的盐酸应加入________mL;
(4)若用0.01mol/LH2SO4应加入_____mL。
4、选择题 (原创题)25℃时,水的电离平衡:H2O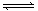 H++OH―?△H>0,下列叙述正确的是(?????)
H++OH―?△H>0,下列叙述正确的是(?????)
A.向水中加入稀氨水,平衡逆向移动,c(OH―)降低
B.向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变
C.向水中加入少量固体NaOH,平衡逆向移动,c(OH―)降低
D.将水加热,Kw增大,c(H+)不变
5、填空题 (8分)在t℃时,某NaOH稀溶液中,c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:
(1)该温度下,水的离子积常数kw=???????。
(2)在该温度下,将100mL0.1mol/L的稀硫酸与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=????。
(3)该温度下,若1体积pH1=a的某强酸溶液与10体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,a和b之间应满足的关系是??????????。(列出含a、b的式子)
(4)该温度下,pH=2的某酸HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5。试分析其原因???????????????????????????????????????????。