微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 广义的水解观认为:无论是盐的水解还是非盐的水解,其最终结果是反应中各物质和水分别解离成两部分,然后两两重新组合成新的物质。根据上述信息,下列说法中不正确的是[???? ]
A.CaO2的水解产物是Ca(OH)2和H2O2
B.PCl3的水解产物是HClO和PH3
C.NaClO的水解产物之一是HClO
D.Mg3N2的水解产物是两种碱性物质
参考答案:B
本题解析:
本题难度:一般
2、填空题 (共8分)
(1)物质的量浓度相同的①氨水;②氯化铵;⑧碳酸氢铵;④硫酸氢铵;⑤硫酸铵5种溶液中c(NH4+)的大小顺序是______,溶液pH的大小顺序是______。
(2)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其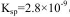 ..CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为
..CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为 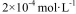 ,则生成沉淀所需CaCl2溶液的最小浓度为 。
,则生成沉淀所需CaCl2溶液的最小浓度为 。
(3)己知: 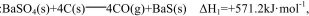
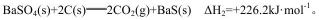
则反应 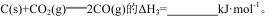
参考答案:每空2分,共8分
(1)⑤>④>②>③>①
本题解析:
试题分析:(1)一水合氨是弱电解质,在水溶液中部分电离,所以浓度相同的这几种溶液中,氨水的铵根离子浓度最小,硫酸铵中铵根离子个数是2,所以硫酸铵中铵根离子浓度最大,碳酸氢根离子促进铵根离子水解、氢离子抑制铵根离子水解,所以氯化铵、碳酸氢铵、硫酸氢铵中铵根离子浓度大小顺序是④>②>③,则相同浓度的这几种溶液中c(NH4+)的由大到小顺序是⑤>④>②>③>①;一水合氨是弱碱,溶液呈碱性,溶液碱性最强;硫酸氢铵溶液为强酸性溶液,pH最小,碳酸氢根离子促进铵根离子水解,硫酸铵中铵根离子水解个数大于氯化铵,所以相同浓度的这几种溶液中,溶液pH的由大到小顺序是①>③>②>⑤>④;
(2)根据反应Ca2++CO32-=CaCO3,C(Ca2+)・C(CO32-)=2.8×10-9,C(Ca2+)= 2.8×10-9/1=2.8×10-9mol/L,由于是等体积的CaCl2溶液与Na2CO3溶液混合,所以生成沉淀所需CaCl2溶液的最小浓度为2.8×10-9mol/L×2=5.6×10-5mol・L-1 ;
(3)根据盖斯定律,(△H1-△H2)÷2=(+571.2-226.2)÷2=+172.5。
考点:考查盐类水解,PH值的大小比较,沉淀溶解平衡的应用,盖斯定律的应用等知识。
本题难度:一般
3、选择题 相同物质的量浓度的NaCN和NaClO相比,NaCN溶液的pH较大,则同温同体积同浓度的HCN和HClO说法正确的是
A.酸根离子浓度:c(CN-)<c(ClO-)
B.pH:HClO>HCN
C.与NaOH恰好完全反应时,消耗NaOH的物质的量:HClO>HCN
D.电离程度:HCN>HClO
参考答案:A
本题解析:
本题难度:简单
4、选择题 某种一元酸(HA)溶液中加入一定量的一种强碱(MOH)溶液后,恰好完全反应,则有关反应后溶液的判断中一定正确的是
A.[A-]≤[M+]
B.[A-]≥[M+]
C.若反应生成的MA不水解,则[A-]>[OH-]
D.若反应生成的MA水解,则[A-]<[OH-]
参考答案:AC
本题解析:本题中的一元酸可能是强酸或弱酸。若是HA为一元强酸与强碱完全中和时,[A-]=[M+],若HA为一元弱酸与强碱完全中和生成的MA为强碱弱酸盐,由于A-发生部分水解反应,[A-]<[M+],故A选项结论[A-]≤[M+]正确,而B选项不正确。若反应生成的MA不水解,即MA为强酸强碱盐,它电离出的[A-]一定大于由水电离出的[OH-]浓度,C选项也正确。
若是反应生成的MA能发生水解,说明HA必然是弱酸,MA为强碱弱酸盐,A-将发生水解:A-+H2O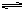 HA+OH-,多数情况[A-]>[OH-],D选项的结论正相反。
HA+OH-,多数情况[A-]>[OH-],D选项的结论正相反。
本题难度:困难
5、选择题 水中加入下列溶液对水的电离平衡不产生影响的是( )
A.NaHSO4溶液
B.KF溶液
C.KAl(SO4)2溶液
D.NaI溶液
参考答案:D
本题解析:A项中电离出的H+抑制水的电离;B项中F-水解促进水的电离;C项中Al3+水解促进水的电离;D项中NaI为强酸强碱盐,对水的电离无影响
本题难度:一般