微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知氯化铁溶液跟铜反应生成氯化铜和氯化亚铁。电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是??????????,证明Fe3+存在的现象是?????????????。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式(1分):????????????????????
(3)某工程师为了从使用过的腐蚀废液中回收铜,并重新获得FeCl3溶液,准备采用下列步骤:
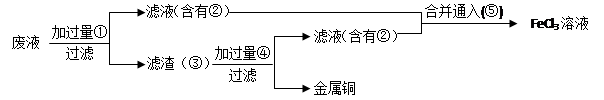
A.请写出上述实验中加入或生成的有关物质的化学式:
①?????????????,②???????????,④????????????,
B.请写出含有②的滤液与⑤反应的离子方程式(1分):??????????????????????????????????
该反应中氧化剂为???????????还原剂为???????????。
参考答案:(9分)(1)KSCN;溶液呈红色 ;(2) 2Fe3++C
本题解析:
试题分析:(1)铁离子能和KSCN溶液发生显色反应,溶液显红色,所以检验溶液中Fe3+存在的试剂是能和KSCN溶液。
(2)氯化铁能和氧化金属铜,反应的离子方程式是2Fe3++Cu=2Fe2++Cu2+。
(3)要从废液中回收金属铜,则需要加入还原剂铁粉,即①是Fe。过滤后生成的滤液是氯化亚铁,即②是氯化亚铁。而滤渣中含有铜和剩余的铁,则需要加入稀盐酸溶解铁,即④是HCl。滤液中含有氯化亚铁,要转化为氯化铁,则需要通入氯气将氯化亚铁氧化生成氯化铁即可。
点评:该题是高考中的常见题
本题难度:一般
2、计算题 将6g纯铁粉加入200mLFe2(SO4)3和CuSO4的混合溶液中充分反应后得到200mL0.5mol/L的FeSO4溶液和5.2g固体,求:
 (1)反应后生成铜多少克?
(1)反应后生成铜多少克?
 (2)加入铁粉前Fe2(SO4)3物质的量浓度。
(2)加入铁粉前Fe2(SO4)3物质的量浓度。
参考答案:(1)2.56g(2)0.1mol/L
本题解析: 发生反应的化学方程式为:
发生反应的化学方程式为:
 ①Fe+Fe2(SO4)3=3FeSO4???????②Fe+CuSO4=Cu+F
①Fe+Fe2(SO4)3=3FeSO4???????②Fe+CuSO4=Cu+F
本题难度:一般
3、选择题 己知:Cu+2Fe3+=2Fe2++Cu2+。现把相同物质的量的CuSO4、FeCl3和Zn置于水中充分反应,反应器中所得混合物除含有SO2-4和Cl-外,还含有
A.Zn2+、Cu、Fe3+
B.Zn、Cu2+、Fe3+
C.Zn2+、Cu2+、Fe、Fe2+
D.Zn2+、Cu、Cu2+、Fe2+
参考答案:D
本题解析:略
本题难度:简单
4、填空题 (l4分)粉末状试样A是由等物质的量的MgO和Fe2O3组成的混合物。进行如下实验:
①取适量A进行铝热反应,产物中有单质B生成;
②另取20 g A全部溶于0.2 L? 6.0 mol・ 盐酸中,得溶液C;
盐酸中,得溶液C;
③将①中得到的单质B和溶液C反应,有气体放出,同时生成溶液D,还残留有固体物质B。请回答:
(1)①产物中的单质B是__________________。
(2)②中所发生的各反应的化学方程式是___________________________________。
(3)③中所发生的各反应的离子方程式是_________________________________。
(4)若溶液D的体积仍视为0.2L,则该溶液中c(Mg2+)为__________________,
c(Fe2+)为___________________。
参考答案: 本题解析:略
本题解析:略
本题难度:一般
5、选择题 将几滴KSCN(SCN-是“类卤素离子”)溶液加入酸性的含有Fe3+的溶液中,溶液变成红色,将该红色溶液分为两份,①一份中加入适量KMnO4溶液,红色褪去;②向另一份中通入SO2,红色也褪去。下列说法不正确的是[???? ]
A.①红色褪去的原因是KMnO4将SCN-氧化,使Fe(SCN)3消失
B.②红色褪去的原因是SO2将Fe3+还原为Fe2+
C.②红色褪去的原因是SO2将SCN-还原
D.SCN-在适当条件下可失去电子被氧化剂氧化为(SCN)2
参考答案:C
本题解析:
本题难度:简单