��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��1.92gCu��һ������ŨHNO3��Ӧ������Cu�IJ��ϼ��٣���Ӧ�����������ɫ��dz����Cu��Ӧ���ʱ�����ռ�������1.12L����״��������Ӧ������HNO3�����ʵ���Ϊ��������
A��1mol
B��0.05mol
C��1.05mol
D��0.11mol
�ο��𰸣�D
���������
���������ͭ�����ᷴӦ������Ũ�ȵļ��٣�����Ļ�ԭ����ļ�̬Խ�ͣ�ͭ��Ũ���ᷴӦ����NO2������ϡ���ᷴӦʱ������NO�������ɵ�������NO2��NO����n��NO2��+n��NO��= 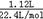 =0.05mol��������ԭ����������ʵ���Ϊ0.05mol��
=0.05mol��������ԭ����������ʵ���Ϊ0.05mol��
n��Cu��=  =0.03mol��������n��Cu��NO3��2��=0.03mol��
=0.03mol��������n��Cu��NO3��2��=0.03mol��
��֪�������Ե���������ʵ���Ϊ0.03mol��2=0.06mol��
��μӷ�Ӧ����������ʵ���Ϊ��0.05mol+0.06mol=0.11mol��
��ѡD��
���㣺��ѧ����ʽ���йؼ���
���������⿼�黯ѧ����ʽ�ļ��㣬������ɲ�ͬ��д�йط�Ӧ�ķ���ʽ��ע��Ũ�����ϡ��������ʵIJ�ͬ���������غ�ĽǶȽ����⡣
�����Ѷȣ�һ��
2��ѡ���� ��NA��ʾ�����ӵ�������ֵ������˵������ȷ����(???? )
A��1 mol N2�����е�ԭ����ΪNA
B����״���£�22.4 Lˮ�к��е�ˮ������ΪNA
C����״���£�22.4 L�Ȼ���������ԭ����ΪNA
D��32 g O2��������ԭ����ĿΪ2NA
�ο��𰸣�D
������������鰢���ӵ�������Ӧ�á��������Ӻ���2����ԭ�ӣ�����1 mol N2�����е�ԭ����Ϊ2NA��ѡ��A����ȷ����״���£�ˮ�������壬��������������Ħ�������ѡ��B����ȷ���Ȼ��⺬��2��ԭ�ӣ����Ա�״���£�22.4 L�Ȼ���������ԭ����Ϊ2NA��ѡ��C����ȷ��32g���������ʵ�����1mol�����Ժ���2mol��ԭ�ӣ�ѡ��D��ȷ����ѡD��
�����Ѷȣ�һ��
3��ѡ���� ��4�֣���2012?�㶫����nAΪ�����ӵ���������ֵ������˵����ȷ���ǣ�������
A�������£�4g CH4��nA��C��H���ۼ�
B��1 mol Fe������ϡHNO3��Ӧ��ת�Ƹ�2nA������
C��1L 0.1 mol/L NaHCO3��Һ�к���0.1nA��HCO3��
D�����³�ѹ�£�22.4L��NO2��CO2������庬��2nA��Oԭ��
�ο��𰸣�A
���������A�������������ʵ�����ϼ�����ӽṹ����̼�����
B������ϡ����������Ӧ������������
C��̼���������ˮ�⣻
D����������Ħ�������Ӧ�������DZ�״��������
�⣺A��4g CH4���ʵ���Ϊ0.25mol�������к�C��H���ۼ�4��0.25��nA=nA������A��ȷ��
B��ϡ���������������������ת�Ƶ���Ӧ����3 nA�����ӣ���B����
C��̼���������ˮ�⣬Ӧ����С��0.1nA��HCO3������C����
D����������ӦΪ��״������D����
��ѡA��
����
�����Ѷȣ�һ��
4��ѡ���� ����������ȷ���ǣ� ��
A����28 g CO������ͬ��������CO2������һ����44 g
B����V L CO������ͬ��������CO2�������һ����V L
C�����������ԭ������CO��CO2��������֮��Ϊ28��11
D���������̼ԭ������CO��CO2�����ܶ�֮��Ϊ21��22
�ο��𰸣�A
���������
���������A��28gCO�����ʵ�����1mol����CO������ͬ�ķ�����Ҳ�Ǿ�����ͬ�����ʵ���������1mol������̼��������44g����ȷ��B����V L CO������ͬ��������CO2���������һ����V L��δָ����ͬ����������C�����������ԭ������CO��CO2�����ʵ���֮����2:1������������2��28:44=14:11������D���������̼ԭ������CO��CO2�����ʵ�����ȣ����������ȷ���������ܶȲ���ȷ��������ѡA��
���㣺���鰢��٤�����ɵ�Ӧ��
�����Ѷȣ�һ��
5��ѡ���� �����͵�����ɵĻ�����������������ܶȿ����ǣ���
A��12.5
B��18.2
C��16.1
D��15.3
�ο��𰸣�D
�����������ν����ܶ���ָ��ͬ�¡�ͬѹ�£�����A�������ǵ�һ���壬Ҳ�����ǻ�����壩���ܶ�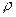 (A)������B�������ǵ�һ���壬Ҳ�����ǻ�����壩���ܶ�
(A)������B�������ǵ�һ���壬Ҳ�����ǻ�����壩���ܶ�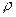 �����Ѷȣ���
�����Ѷȣ���