微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 2011年8月12日,《云南信息报》首度披露?了云南曲靖铬污染事件,引起全国广泛关注.工业上将制取重铬酸钾(K2Cr2O7)和铬酸酐(CrO3)的剩余废渣称为铬渣,其成分为:SiO2、Al2O3、MgO、Fe2O3、CrO3、K2Cr2O7等.
已知:①重铬酸钾和铬酸酐都易溶于水,这是造成铬污染的主要原因,它们都是强氧化剂,铬酸酐溶于水呈酸性;
②+6价铬易被人体吸收,可致癌:+3价铬不易被人体吸收,毒性小.
③下表为一些金属氢氧化物沉淀的pH参照数据.
| 物质 | ?开始沉淀 | ?完全沉淀
?Fe(OH)3
?2.7
?3.7
?Al(OH)3
?3.7
?4.7
?Cr(OH)3
?4.7
?a
?Fe(OH)2
?7.6
?9.6
?Mg(OH)2
?9.6
?11.1
回答下列处理铬渣、消除铬污染的有关问题:
(1)将铬渣用稀硫酸浸取、过滤,在浸出液中加入适量的绿矾(FeSO4?7H2O),加入绿矾的目的是______.
(2)再向浸出液中缓慢加入烧碱,至pH刚好达到4.7,过滤,所得沉淀的化学式是______;常温下,Cr(OH)3的溶度积Ksp=10-32,要使Cr3+完全沉淀[c(Cr3+)降至10-5mol?L-1视为沉淀完全],溶液的pH应调于a=______.
(3)向(2)中得到的滤液中加入硫酸,调节至呈强酸性,所得的溶液是含______溶质的溶液.
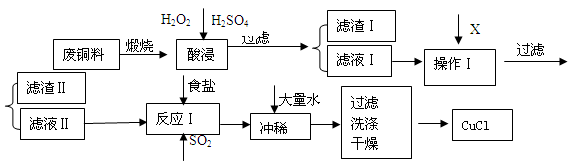
2、简答题 (14分) CuCl是有机合成的重要催化剂,并用于颜料、防腐等工业。工业上由废铜料(含Fe、Al及其化合物、SiO2杂质),生产CuCl的工艺流程如下:
|