微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列元素中,属于第三周期的是
A.氮
B.氟
C.硅
D.钾
参考答案:C
本题解析:试题分析:周期数=电子层数,根据核外电子排布可知氮和氟是第二周期元素,硅是第三周期元素,钾是第四周期元素,答案选C。
考点:考查元素周期表的结构
点评:该题是基础性试题的考查,难度不大。明确元素周期表的编制原则和元素原子的核外电子排布是答题的关键。
本题难度:困难
2、选择题 石墨烯是仅由一层碳原子构成的新型材料,具有超强的导电性。下列元素与碳元素处于同一主族的是
A.He
B.O
C.Si
D.P
参考答案:C
本题解析:试题分析:碳元素的最外层电子数是4个,属于第ⅣA族元素,选项C正确,He是0族,O是第ⅥA族元素,P是第ⅤA族元素,答案选C。
考点:考查元素周期表的结构
点评:该题是高考中的常见考点,属于基础性试题的考查,有利于培养考查学生灵活运用基础知识解决实际问题的能力,也有助于调动学生学习化学的兴趣和学习积极性。该题的关键是记住元素周期表的结构,然后结合题意灵活运用即可。
本题难度:一般
3、选择题 下列分子或离子的空间构型为平面三角形的是
A.SiH4
B.H3O+
C.SO32-
D.NO3-
参考答案:D
本题解析:试题分析:立体构型为平面三角形的分子应含有3个δ键,且没有孤对电子,中心原子为sp2杂化,据此将进行解答。A、Si原子形成4个δ键,根据价层电子对互斥理论可知孤对电子数=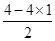 =0,所以为s p3杂化,立体构型为正四面体,因此A不选;B、O原子形成3个δ键,孤对电子数=
=0,所以为s p3杂化,立体构型为正四面体,因此A不选;B、O原子形成3个δ键,孤对电子数=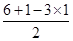 =1,所以为sp3杂化,立体构型为三角锥型,故B不选;C、S原子形成3个δ键,孤对电子数=
=1,所以为sp3杂化,立体构型为三角锥型,故B不选;C、S原子形成3个δ键,孤对电子数=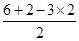 =1,所以为sp3杂化,立体构型为三角锥型,故C不选;D、N原子形成3个δ键,孤对电子数=
=1,所以为sp3杂化,立体构型为三角锥型,故C不选;D、N原子形成3个δ键,孤对电子数=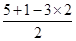 =0,所以中心原子为sp2杂化,立体构型为平面三角形,故D正确,答案选D。
=0,所以中心原子为sp2杂化,立体构型为平面三角形,故D正确,答案选D。
考点:考查分子空间构型的判断
本题难度:困难
4、选择题 下列各组物质仅用溴水即可鉴别的是
A.苯、己烷、己烯
B.己烷、己烯、二甲苯
C.苯、四氯化碳、己炔
D.甲苯、四氯化碳、己烯
参考答案:C
本题解析:A组物质中,己烯与溴单质发生加成反应,溴水褪色;苯和己烷与溴水均可分层,且有色层均在上层,不能鉴别.B组物质中,二甲苯与溴水发生萃取,有机层在上层,为有色层,下层为水层,为无色层,同己烷与溴水发生萃取的现象相同,不能鉴别.同理,D组物质也不能鉴别.C组物质中,己炔能使溴水褪色,苯和四氯化碳均不与溴水发生化学反应,但二者均能萃取溴水中的溴单质,而使得混合液分层,根据密度差异,可知,苯和溴水的混合液中,苯在上层,为有色层,而四氯化碳和溴水的混合液中,四氯化碳在下层,为有色层,可以鉴别.
本题难度:简单
5、选择题 下列哪些实验事实不能说明有分子间作用力的存在
A.甲烷燃烧放出大量的热
B.液氯汽化要吸收一定的能量
C.降低温度氯气会凝结成液态
D.增加压强CO2会凝结成固态
参考答案:A
本题解析:甲烷燃烧放出大量的热是因为断开化学键是需要吸收能量,而形成化学键时需要放出能量,它们之间的差值属于反应热,即反应热与分子间作用力无关。氯气和CO2均属于分子晶体,分子间存在分子间作用力,主要影响物质的物理性质,所以选项BCD和分子间作用力有关。答案是A。
本题难度:困难