��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪��Ӧ3S��6KOH(Ũ) 2K2S��K2SO3��3H2O����Ӧ���������ͻ�ԭ������������?(???? )?��
2K2S��K2SO3��3H2O����Ӧ���������ͻ�ԭ������������?(???? )?��
A��3��1
B��1��3
C��2��1
D��1��2
�ο��𰸣�C
�������������������ԭ��Ӧ���й��жϺͼ��㡣����Ԫ�ػ��ϼ۵ı仯��֪����������ǻ�ԭ����Ҳ��������������2mol��Ļ��ϼ���0�۽��͵���2�ۣ���������������1mol���ϼ۴�0�����ߵ���4�ۣ�����ԭ��������������ͻ�ԭ��������֮����2�U1����ѡC��
�����Ѷȣ�һ��
2��ѡ���� �������ǿ�������·ֽ⣬���ɰ���������������ˮ����Ӧ�����ɵ���������ͻ�ԭ��������ʵ���֮���ǣ�????��
A��1:3
B��2:3
C��1:1
D��4:3
�ο��𰸣�B
���������
���������3(NH4)2SO4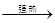 4NH3����3SO2����N2����6H2O
4NH3����3SO2����N2����6H2O
������ɵ���������N2�ͻ�ԭ����SO2�����ʵ���֮����1:3��ѡA��
�����Ѷȣ�һ��
3������� (1)��MnSO4������Ļ����Һ�����K2S2O8(���������)����Һ�лᷢ�����·�Ӧ��Mn2++ S2O82-+H2O��MnO4-+SO42һʮH+�÷�Ӧ�����ڼ���Mn2+�Ĵ��ڡ������������� ������Ӧ����0��1 mol��ԭ���μӷ�Ӧ�������������������ʵ���Ϊ mol��
(2)���÷�Ӧ���õ������̸�Ϊ�Ȼ��̣������������Ĺ�����ط�Ӧʱ�����и�����ء�����ء����������⣬�����������ﻹ�� ��
(3)��NaBiO3����(��ɫ��)���뵽MnSO3��H2SO4�Ļ����Һ����ȣ������ܽ��Ϊ������Һ���������·�Ӧ�� NaBiO3+ MnSO4+ H2S04�� Na2S04+ Bi2(SO4)3+ NaMnO4+ H2O��
����ƽ������Ӧ�Ļ�ѧ����ʽ��
��������Ӧ�л�ԭ������ ��
���õ����ű�ʾ��������ԭ��Ӧ ��
��4��S2O82-��һ�������£���ת��ΪS2O32-��д����K2S2O3�еμ�ϡ��������ӷ���ʽ�� ��
�ο��𰸣�(1)��Һ����ɫ��Ϊ��ɫ��0.25 &
���������
�����������1��MnO4-Ϊ��ɫ���������Ӿ�Ϊ��ɫ����Ӧ������Ϊ��Һ����ɫ��Ϊ��ɫ��MnԪ�صĻ��ϼ����ߣ�SԪ�صĻ��ϼ۽��ͣ���0.1mol��ԭ����MnSO4���μӷ�Ӧ�������������������ʵ���Ϊ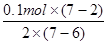 ��0.25mol��
��0.25mol��
��2�������̸�Ϊ�Ȼ��̣������������Ĺ�����ط�Ӧʱ�������ӿ��ܱ�����������и�����ء�����ء����������⣬�����������ﻹ��Cl2��
��3����BiԪ�صĻ��ϼ���+5�۽���Ϊ+3�ۣ�MnԪ�صĻ��ϼ���+2������Ϊ+7�ۣ���ϵ����غ㡢ԭ���غ��֪����ӦΪ10NaBiO3+4MnSO4+14H2S04��3Na2S04+5Bi2��SO4��3+4NaMnO4+14H2O���ʴ�Ϊ��10��4��14��3��5��4��14��
��BiԪ�صĻ��ϼ۽��ͣ�����ԭ����Ӧ��ԭ����ΪBi2��SO4��3��
��Mnʧȥ���ӣ�Bi�õ����ӣ��÷�Ӧ��ת��20e-���õ����ű�ʾ��������ԭ��ӦΪ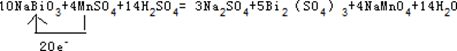 ��
��
��4��K2S2O3�еμ�ϡ���ᣬ����������ԭ��Ӧ��������ء�S�����������ˮ�����ӷ�ӦΪS2O32-+2H+��S��+SO2��+H2O���ʴ�Ϊ��S2O32-+2H+=S��+SO2��+H2O��
���㣺����������ԭ��Ӧ���й��ж������
�����Ѷȣ�һ��
4������� ��һ�ٶ��ֻ�ѧԪ���У��ǽ���ռ��23�֡�80%�ķǽ���Ԫ���������ռ��Ҫλ�á���C��N��O��Si��Cl�ȡ�
��1����Ԫ��ԭ��������Ӳ�����???��������ͬ�ĵ��ӣ���Ԫ�صļ������Ӻ�������Ų�ʽ��??????????????????��
��2���ɵ�Ԫ�����Ԫ����ɵ����ʣ����������췢���������Ȳ�������Ϊ������???????���壬��д���û�����Ļ�ѧʽ????????????��
��3��������ʵ��˵����������Ԫ�طǽ��������ǿ������???????????����ѡ���ţ�
a��Clԭ������������������
b�����ԣ�HCl��H2O
c��ClO2����Ԫ��Ϊ+4�ۣ���Ԫ��Ϊ?2��
d���е㣺H2O��HCl
��Cl2��Ƚϣ�ClO2����ˮʱ����ԭ��Cl�����������л��ȴ�����к����ʡ���ҵ�Ͽ����������ƺ�ϡ����Ϊԭ���Ʊ�ClO2����Ӧ���£�NaClO2 +HCl ClO2��+___________________��û����ƽ��
ClO2��+___________________��û����ƽ��
��4����������ʽ�У�ȱ��������___________����ƽ����ʽ���������油ȫ��Ӧ��ϵ����____NaClO2 +____HCl
��5���÷�Ӧ���������ͻ�ԭ�������ʵ���֮����???????������0.2 mol ClO2ת�Ƶ��ӵ����ʵ���Ϊ_______ mol��
��6��ClO2����ˮ��Fe2����Mn2����S2����CN���������Ե�ȥ��Ч����ij��ˮ�к�CN��a mg/L������ClO2��CN��������ֻ�������������塣����100m3������ˮ��������ҪClO2 _______ mol ��
�ο��𰸣���1��2?? 1s22s22p63s23p6
��2��ԭ
���������
�����������1����Ԫ��ԭ��������Ӳ�����Ų�ʽΪ3S2P5������2��������ͬ�ĵ��ӣ���Ԫ�صļ������Ӻ�������Ų�ʽ��[Ne]3S23P6��
��2���ɵ�Ԫ�����Ԫ����ɵ����ʣ����������췢���������Ȳ�����˵���۵�ܸߣ�����ԭ�����壬���ݻ��ϼۣ��û�����Ļ�ѧʽ Si3N4��
��3��a������ͨ��Clԭ�����������������ֻ࣬��ͨ���õ��ӵ�������˵��������bӦ������������Ӧˮ���������ǿ���Աȣ��������⻯��ˮ��Һ�����ԶԱȣ�����c��ClO2����Ԫ��Ϊ+4
�����Ѷȣ�һ��
5��ѡ���� ����Fe2����I����Br������Һ��ͨ��������������Һ�и������ӵ����ʵ����仯��ͼ��ʾ���й�˵������ȷ����
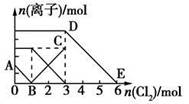
A���߶�BC����Fe3�����ʵ����ı仯���
B��ԭ�����Һ��n(FeBr2)��3 mol
C����ͨ��2 mol Cl2ʱ����Һ���ѷ��������ӷ�Ӧ�ɱ�ʾΪ��
2Fe2����2I����2Cl2===2Fe3����I2��4Cl��
D��ԭ��Һ��n(Fe2��):n(I��):n(Br��)��3:1:2
�ο��𰸣�D
������������⿼���˻�ѧͼ��Ԫ�ػ���������ʡ�������ԭ��Ӧ����ѧ����ȣ����ڿ��鿼����ʶͼ������������������ԭ��˳��Br��<Fe2��<I�������ݻ�ѧͼ��Ӧԭ��֪���߶�AB����I�����ʵ����ı仯������߶�BC����Fe3�����ʵ����ı仯������߶�DE����Br�����ʵ����ı仯�����A����ȷ������ͼ������������������֪��ԭ��Һ��n(I��)��2 mol��n(Fe2��)��4 mol��n(Br��)��6 mol��n(Fe2��):n(I��):n(Br��)��2:1:3��D�����n(FeBr2)��3 mol��n(F
�����Ѷȣ�һ��