微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 右图为番茄制作的水果电池,下列说法正确的是
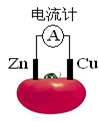
A.一段时间后,铜片质量减小
B.锌电极发生氧化反应
C.电流由锌通过导线流向铜
D.铜电极是该电池的负极
参考答案:B
本题解析:
试题分析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌的金属性强于铜的,所以锌是负极,铜是正极,溶液中的氢离子在正极得到电子生成氢气,所以选项B正确,其余选项都是错误的,答案选B。
点评:该题是基础性试题的考查,试题注重基础,贴近生活,有利于调动学生的学习积极性。该题的关键是明确原电池的工作原理,特别是正负极的判断以及和电极反应式的书写。
本题难度:一般
2、选择题 电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3胶体。Fe(OH)3有吸附性,可吸附污物使之沉积下来,具有净化水的作用。模拟处理装置如图所示,下列说法错误的是( )
A.X电极是负极,电极反应式为CH4-8e-+4CO32-=5CO2+2H2O
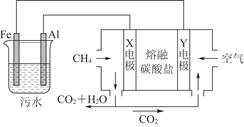
B.铁作阳极,失去电子生成Fe2+
C.工作时熔融盐中的碳酸根移向Y电极
D.污水中存在反应4Fe2++10H2O+O2=4Fe(OH)3↓+8H+
参考答案:C
本题解析:结合“电解生成Fe(OH)3胶体”,说明Fe作阳极失电子形成Fe2+,在空气中转化成Fe(OH)3,那么Y作正极,X作负极,A、B、D项正确,结合A项,CO32-向X电极移动,C项错误。
本题难度:一般
3、选择题 直接提供电能的反应一般是放热反应,下列反应中能直接提供电能的是(??)
A.Ba(OH)2・8H2O与NH4Cl反应
B.氢氧化钠与稀盐酸反应
C.灼热的炭与CO2反应
D.H2与O2的反应
参考答案:D
本题解析:
试题分析:一般氧化还原反应才能设计成原电池,提供电能。据此可知选项AB不正确,二者都是非氧化还原反应,C是氧化还原反应,但是吸热反应,答案选D。
点评:该题是中等难度的试题,侧重对学生基础知识的巩固和检验,难度不大。该题的关键是明确常见的放热反应和吸热反应,以及氧化还原反应的判断,有利于培养学生的逻辑推理能力。
本题难度:简单
4、填空题 某学生利用下面实验装置探究盐桥式原电池的工作原理(Cu元素的相对原子质量为64)。
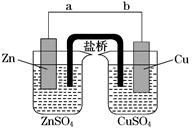
按照实验步骤依次回答下列问题:
(1)导线中电子流向为__________________(用a、b表示)。
(2)写出装置中锌电极上的电极反应式:____________________________________;
(3)若装置中铜电极的质量增加0.64 g,则导线中转移的电子数目为________;(不许用“NA”表示)
(4)装置的盐桥中除添加琼脂外,还要添加KCl的饱和溶液,电池工作时,对盐桥中的K+、Cl-的移动方向的表述正确的是________。
A.盐桥中的K+向左侧烧杯移动、Cl-向右侧烧杯移动
B.盐桥中的K+向右侧烧杯移动、Cl-向左侧烧杯移动
C.盐桥中的K+、Cl-都向左侧烧杯移动
D.盐桥中的K+、Cl-几乎都不移动
参考答案:(1)由a到b(或a→b)
(2)Zn-2e-=Zn2
本题解析:在该原电池中负极为Zn,电极反应为Zn-2e-=Zn2+,正极为铜,电极反应为Cu2++2e-=Cu,当铜电极增加0.64 g时,转移电子(由a到b)为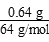 ×6.02×1023 mol-1×2=1.204×1022。盐桥中K+向正极区(右侧烧杯)移动,Cl-向负极区(左侧烧杯)移动。
×6.02×1023 mol-1×2=1.204×1022。盐桥中K+向正极区(右侧烧杯)移动,Cl-向负极区(左侧烧杯)移动。
本题难度:一般
5、填空题
请根据反应 Fe + CuSO4=FeSO4 + Cu,设计原电池,完成以下问题。
负极:_______________ ,其电极反应式为:_______________________________
正极:_______________ ,其电极反应式为:_______________________________
电解质溶液:___________,电池的离子反应式为:_______________________________
参考答案:负极:Fe;其反应为:Fe-2e-==Fe2+;正极:Cu(
本题解析:
本题难度:一般