0.012
?
(1)判断反应达到平衡状态的依据是(??)
A.混合气体的密度不变
B.混合气体的平均相对分子质量不变
C.生成CH3OH的速率与消耗CO的速率相等
D.CH3OH、CO、H2的浓度都不再发生变化
(2)由表中数据判断Q????????0 (填“>”、“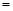 ”或“<”),要提高CO转化率,可采取的措施 ”或“<”),要提高CO转化率,可采取的措施
是(??)
A.加入催化剂?????? B.充入CO?????? C.充入H2????? D.升温
(3)某温度下,将2 mol CO和6 mol H2充入2 L的密闭容器中,充分反应10min后,达到平衡时测得c mol/L,则以CH3OH表示的反应速率v mol/L,则以CH3OH表示的反应速率v ???????????mol /(L・min), ???????????mol /(L・min),
CO的转化率为???????????????。
(4)原料CO和H2可以由C和H2O反应制取,涉及的反应方程式如下:
C(s)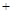 CO2(g) CO2(g)  2CO(g)??????????????平衡常数K1 2CO(g)??????????????平衡常数K1
C(s)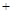 H2O(g) H2O(g)  CO(g) CO(g)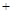 H2(g)?????????平衡常数K2 H2(g)?????????平衡常数K2
CO(g)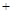 H2O(g) H2O(g)  H2(g) H2(g)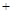 CO2(g)???????平衡常数K3 CO2(g)???????平衡常数K3
则K1、K2、K3之间的关系是:???????????????????????。
参考答案:
(1)BD ?(2分)
(2)>(1分)
本题解析:
试题分析:
(1)A恒容密闭容器,体积不变,都是气体,质量守恒,混合气体的密度始终不变,不能做平衡标志,错误;B正确;C生成CH3OH和消耗CO的速率是同向速率,错误;D正确。
(2)由表可知,T升高,K减小,正反应是放热反应,Q>0。提高CO转化率,反应正向进行,选C。
(3)?CO(g)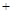 2H2(g) 2H2(g)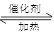 CH3OH(g) CH3OH(g)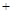 Q Q
初浓度:? 1??? 3?????????????? 0
变浓度?? 0.8?? 1.6???????????? 0.8????
平衡???? 0.2
v 0.8/10=0.08(mol/L・min) 0.8/10=0.08(mol/L・min)
CO的转化率=" 0.8" /1*100%= ?80%
(4)①C(s)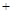 CO2(g) CO2(g)  2CO(g)?????平衡常数K1 2CO(g)?????平衡常数K1
②C(s)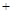 H2O(g) H2O(g)  CO(g) CO(g)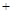 H2(g)?????平衡常数K2 H2(g)?????平衡常数K2
③CO(g)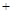 H2O(g) H2O(g)  H2(g) H2(g)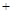 CO2(g)???平衡常数K3 CO2(g)???平衡常数K3
②=①+③ 所以K2=K1・K3
本题难度:一般
2、选择题 反应CO(g)+H2O(g)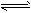 CO2(g)+H2(g) ΔH=-41.2 kJ・mol-1,在800℃时的化学平衡常数 CO2(g)+H2(g) ΔH=-41.2 kJ・mol-1,在800℃时的化学平衡常数
K=1.0 。某时刻测得该温度下的密闭容器中各物质的物质的量见下表

此时反应中正、逆反应速率的关系式是 [???? ]
A.v(正)>v(逆)
B.v(正)<v(逆)
C.v(正)=v(逆)
D.无法判断
参考答案:A
本题解析:
本题难度:一般
3、选择题 把镁带投入盛有稀HCl的容器里,产生H2的速率与下列因素有关系的是
①盐酸的浓度;②温度;③镁带的表面积;④容器的密闭情况;⑤溶液的氯离子浓度
A.①②
B.③④
C.①②③④
D.①②③④⑤
参考答案:C
本题解析:反应的实质是Mg(s)+2H+==Mg2++H2↑;ΔH<0,反应速率除与氯离子浓度无关外,其他四个因素对反应速率都有影响。
本题难度:一般
4、填空题 (8分)在一定条件下,将3molA 和1mol B 两种气体混合于固定容积为2L的密闭容器中,发生如下反应:3A(g)+B(g) ?xC(g)+ 2D(g)。2min末该反应达到平衡,生成0.8mol D ,并测得C的浓度为0.2mol・L-1。请填空: ?xC(g)+ 2D(g)。2min末该反应达到平衡,生成0.8mol D ,并测得C的浓度为0.2mol・L-1。请填空:
(1)x=__________(有过程)
(2)温度降低,K值增大,则正反应是_________(填“放热”或“吸热”)反应。
(3)B的转化率为_____????____(有过程)。
(4)能判断该反应达到平衡状态的依据是________(填编号)
A.混合气体的密度不变
B.容器中的压强不再变化
C.生成D的反应速率是生成B的反应速率的2倍
D.单位时间内生成3molA,同时生成1molB
参考答案:(1) 1??????(2)放热???(3)40%??(4)
本题解析:(1)C的浓度为0.2mol・L-1,则生成C是0.4mol。根据变化量之比是相应的化学计量数之比可知,x=1。
(2)温度降低,K值增大,说明平衡向正反应方向移动,所以正反应是放热反应。
(3)根据方程式可知,消耗B是0.4mol,所以B的转化率是0.4mol÷1.0mol×100%=40%。
(4)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,A不正确。根据方程式可知,反应是体积减小的,所以压强也是减小的,因此选项B正确。C中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确。D中反应速率的方向是相同的,不正确。答案选BC。
本题难度:一般
5、填空题 在一定温度下有甲、乙两容积相等的密闭容器
(1)向甲容器中通入1mol N2和3 mol H2,反应达到平衡时,生成NH3amol。此时,NH3的质量分数是______。(用含有“a”的表达式表示)。
(2)若起始时(两容器容积保持不变)。,向乙中通入2molN2和6molH2,达到平衡时,生成的NH3的物质的量为b mol,a/b????????????1/2(选填“>”、“<”或“=”)。
(3)若起始时甲保持容积不变,向甲容器中通入1mol N2和3 mol H2,反应达到平衡时,生成NH3amol,而乙保持压强不变, 向乙容器中通入1mol N2和3 mol H2,反应达到平衡时,生成NH3b mol,则a???????????b(选填“>”、“<”或“=”)
参考答案:(1)a/2?(2)<?(3)<
本题解析:考查可逆反应的有关计算。
(1)根据质量守恒定律可知,氨气的质量分数是 。 。
(2)乙相当于在甲的基础上增大压强,根据方程式3H2+N2 2NH3可知,平衡向正反应方向移动,转化率增大,即b>2a,所以a/b<1/2。 2NH3可知,平衡向正反应方向移动,转化率增大,即b>2a,所以a/b<1/2。
(3)由于反应是体积减小的,即压强也是减小的,所以乙中压强大于甲中的。压强大有利于平衡向正反应方向移动,所以a<b。
本题难度:一般
|