微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 高铁酸钾( K2FeO4)是一种集强氧化性、吸附、絮凝于一体的新型多功能水处理剂,生产工艺如下:?

已知:
①温度较低时:2KOH+Cl2=KCl+KClO+H2O
②温度较高时:6KOH+3Cl2=5 KCl+KClO3+3H2O
③Fe(NO3)3+KClO+KOH→K2FeO4+KNO3+KCl+H2O(未配平)
(1)该生产应在温度________的情况下进行(填“较高”或“较低”);
(2)请配平反应③:
?口Fe(NO3)3+口KClO+口KOH→口K2FeO4+口KNO3+口KCl+H2O
(3) K2FeO4具有强氧化性的原因为___________;
(4)在“反应液I”中加KOH固体的目的是____________;
A.为下一步反应提供反应物
B.与“反应液I”中过量的Cl2继续反应,生成更多的KClO
C.KOH同体溶解时会放出较多的热量,有利于提高反应速率
D.使副产物KClO3转化为KClO
(5)从“反应液Ⅱ”中分离出K2FeO4晶体后,可以得到的副产品有 ____(写化学式)。
2、选择题 天然气、液化石油气燃烧的化学方程式分别为:CH4 +2O2 CO2+2H2O, C3H8+5O2
CO2+2H2O, C3H8+5O2 3CO2+4H2O。现有一套以天然气为燃料的灶具,欲改烧液化石油气,应采取的正确措施是 [???? ]
3CO2+4H2O。现有一套以天然气为燃料的灶具,欲改烧液化石油气,应采取的正确措施是 [???? ]
A.两种气体进入量都减少
B.增大空气进入量或减小液化气进入量
C.两种气体进入量都增大
D.减小空气进入量或增大液化气进入量
3、选择题 我国许多城市已经推广使用清洁燃料,如压缩天然气(CNG)类和液化石油气(LPG)类.这两类燃料的主要成分是( )
A.醇类
B.一氧化碳
C.氢气
D.烃类
4、填空题 碘化钠是实验室中常用的分析试剂,也常用于医疗和照相业。工业上用铁屑还原法制备NaI,其主要流程如下图,请回答下列问题
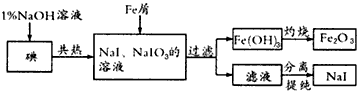
(1)判断碘是否已完全反应的实验方法是____________;
(2)将滤液在低温下分离出NaI样品过程中,要防止NaI被氧化,最好采取的措施是________________;
(3)测定产品中NaI含量的方法是:
a.称取3.000 g样品、溶解,在250 mL容量瓶中定容;
b.量取25. 00 mL待测溶液于锥形瓶中;
c.用0.1 000 mol/LAgNO3溶液滴定至终点,消耗AgNO3溶液体积的平均值为19. 00 mL。
①上述测定过程所需仪器中,需要检查是否漏液的仪器有_____________。
②上述样品中NaI的质量分数为________________
③若用上述方法测定产品中NaI的质量分数偏低(测定过程中产生的误差忽略不计),其可能原因有
______________________
5、填空题 (三选一)【化学与技术】
2011年8月12日,网上传云南曲靖市越州镇有总量5000余吨的重毒化工废料铬渣由于非法丢放,毒水被直接排放南盘江中。
Ⅰ:某工厂对制革工业污泥中Cr(III)回收与再利用工艺如下(硫酸浸取液中金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+、Mg2+)
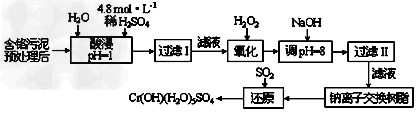
部分阳离子常温下以氢氧化物形式沉淀时溶液的pH见下表
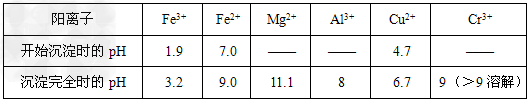
(1)实验室用18.4?mol/L的浓硫酸配制250?mL?4.8?mol/L的硫酸溶液,所用的玻璃仪器除烧杯、玻璃棒和吸量管(一种能精确量取一定体积液体的仪器)外,还需____________。 ??
(2)酸浸时,为了提高浸取率可采取的措施是______________(至少答一点)。?
(3)加入H2O2的作用是__________________________,调节溶液的pH=8是为了除去_________离子。 ??
(4)钠离子交换树脂的原理为:Mn++nNaR→MRn+nNa+,被交换的的杂质离子是____________。
(5)还原过程发生以下反应(请配平):? _____Na2Cr2O7+_____SO2+____???________?=?____?Cr(OH)(H2O)5SO4+_______Na2SO4;
Ⅱ:工业废水中常含有一定量的Cr2O72-和CrO42-,它们会对人类及生态系统产生很大损害,必须进行处理。其中一种处理方法为电解法:该法用Fe做电极,电解含Cr2O72-的酸性废水,随着电解进行,阴极附近溶液pH升高,产生Cr(OH)3沉淀。
(6)阳极的电极反应式为_______________。在阴极附近溶液pH升高的原因是(用电极反应方程式解释)__________。