微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述错误的是 [???? ]
A.乙烯的结构简式为 CH2CH2
B.甲醚的结构式为 
C.甲烷的电子式??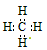
D.邻甲基苯酚的结构简式为 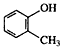
参考答案:A
本题解析:
本题难度:简单
2、填空题 (16分)
快乐是什么?精神病学专家通过实验发现:在大脑的相应部位――“奖赏中心”,给予柔和的电击,便会处于似乎极度快乐的状态.人们已经将“奖赏中心”各部分的脑电图绘制出来,并认为,在各区域之间传递信息的化学物质是多巴胺,所以“奖赏中心”又称为多巴胺系统.
多巴胺结构如图:
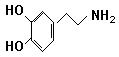
(1)多巴胺分子式:???????????????????????.
(2)试判断多巴胺能发生的化学反应?????????.???????????????????
A.加成
B.取代
C.氧化
D.水解
(3)写出与多巴胺互为同分异构体且满足下列三个条件的所有物质的结构简式:
①属于1、3、5三取代苯????????????????????②苯环上直接连有一个羟基和一个氨基
③分别能与钠和氢氧化钠反应,消耗钠与氢氧化钠的物质的量之比为2:1
??????????????????????????????????????????????????????.??
(4)多巴胺可由香兰素与硝基甲烷缩合,再经锌汞齐还原水解而得.合成过程表示如下:
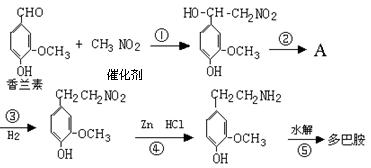
(Ⅰ) 写出下列反应类型:反应①???????????????,反应⑤??????????????????.
(Ⅱ) A的结构简式:????????????????????????????????????????????????????.
(Ⅲ) 写出②的化学方程式:??????????????????????????????????????????????.
参考答案:
(1)C8H11NO2???????(2分)
本题解析:略
本题难度:简单
3、简答题 【选修3物质结构与性质】(15分)
VIA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种氧化态,含VIA族元素的化台物在研究和生产中有许多重要用途。请回答下列问题:
(1)S单质的常见形式为S8,其环状结构如下图所示,S原子采用的轨道杂化方式是??????;
 ?
?
(2)原子的第一电离能是指气态电中性基态原子失去一个电子转化为气态基态正离
子所需要的最低能量,O、S、Se原子的第一电离能由大到小的顺序为???????????????;
(3)Se原子序数为???????,其核外M层电子的排布式为????????????????????;
(4)H2Se的酸性比H2S?????????(填“强”或“弱”)。气态SeO3分子的立体构型
为?????????????????,SO32-离子的立体构型为???????????????????;
(5)H2SeO3的K1和K2分别为2.7x l0-3和2.5x l0-8,H2SeO4第一步几乎完全电离,
K2为1.2X10-2,请根据结构与性质的关系解释:
①H2SeO3和H2SeO4第一步电离程度大于第二步电离的原因:??????????????????????????
???????????????????????????????????????????????????;
② H2SeO4比 H2SeO3酸性强的原因:??????????????????????????????????????????????????
??????????????????????????????????????????????????????????????????????????????
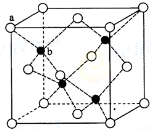
(6)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0 pm.密度为????????????????????(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为???????????????pm(列示表示)
参考答案:(1)SP3
(2)O>S>Se
(3)34??
本题解析:(1)因为S8为环状立体结构,键角为120°,所以轨道杂化方式为SP3。
(2)根据同主族电离能变化规律,O、S、Se原子的第一 电离能由大到小的顺序为O>S>Se.(3)Se原子序数为34,其核外M层电子的排布式为3s23p63d10(4)原子半径越大,氢化物越容易电离出氢离子,所以H2Se的酸性比H2S强。气态SeO3分子的立体构型为正四面体,SO32-离子的立体构型为平面三角形。(5)①H2SeO4和H2SeO3第一步电离产生的氢离子抑制第二步电离,所以第一步电离程度大于第二步电离程度。
本题难度:一般
4、选择题 下列过程中,共价键被破坏的是[???? ]
A.碘升华
B.溴蒸气被木炭吸附
C.酒精溶于水
D.氯化氢气体溶于水
参考答案:D
本题解析:
本题难度:简单
5、填空题 A、B、C、D、E五种短周期元素,F为第四周期过渡元素,核电荷数依次增加。
元素
| 有关性质及结构信息
|
A
| A的一种原子内无中子
|
B
| B原子的电子填充了4个原子轨道
|
C
| C22―离子与电负性最大的元素的单质互为等电子体
|
D
| D是短周期金属性最强的元素
|
E
| C与E同族
|
F
| 外围电子排布式为nd2n(n+1)s(n-1)
|
| |
?
(1)E2-基态核外电子排布式???????????,D单质的晶胞为体心立方,其配位数是???????????,C的氢化物在同族元素中沸点反常,其原因是??????????????。
(2)由A、B两种元素组成的非极性分子有多种,其中乙是一个分子含4个原子的的分子,乙的结构式是???????????。已知1g乙完全燃烧热为46.16 kJ,乙燃烧热的热化学反应方程式是???????????????????。
(3)甲是由A、B、C三种元素组成的相对分子质量最小的物质。甲的中心原子的杂化方式是?????????????。由甲中的两种元素组成,且与甲的电子数相等的物质的分子式是????????,该物质与C的单质在K2CO3溶液中形成燃料电池的负极反应式为????????。
(4)分别由A、C、D、E四种元素中的3种组成的两种物质丙和丁在溶液中反应生成气体和沉淀,该化学方程式是 ??????????????????????????????????。
(5)C与D形成一种物质戊,将过量戊加入过量F与稀硫酸反应后的溶液,得到红褐色沉淀和气体,发生反应的离子方程式是???????????????????????????????。
参考答案:(1)1s22s22p63s23p6,?? 8 ,?????
本题解析:
试题分析:根据给定条件可知这六种元素分别是:A: H;? B :C;? C:O;? D:Na;?? E:S;? F;Fe。(1)S2-基态的核外电子排布式是1s22s22p63s23p6。Na的晶胞是体心立方结构配位数是8.H2O的沸点反常是因为在水分子间除了有一般的分子间作用力外还有氢键存在。增加了分子间的相互作用。使物质融化或汽化消耗的能量增多,所以熔点、沸点反常。(2)有C、H两元素形成的四原子分子是C2H2.它的结构式是H-C≡C-H。乙炔燃烧的热化学方程式是:C2H2(g)+5/2O2(
本题难度:困难
|