微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 水热法制备Fe(FeO2)2纳米颗粒的反应3Fe2++2S2O32-+O2 +xOH-=Fe(FeO2)2+S4O62-+2H2O
下列说法中不正确的是
A.每生成1mol Fe(FeO2)2转移4mol电子
B.该反应中Fe2+和S2O32-都是还原剂
C.3mol Fe2+被氧化时有1molO2被还原
D.反应方程式中化学计量数x=4
参考答案:C
本题解析:
试题分析:A、由反应方程式知,每生成1mol Fe(FeO2)2时1molO2参加反应,转移的电子为4mol,正确;B、该反应中铁元素的化合价由+2价升高到+3价,硫元素的化合价由+2价升高到+2.5价,该反应中Fe2+和S2O32-都是还原剂,正确;C、由反应方程式知,3molFe2+参加反应时只有2mol被氧化,此时该反应中1molO2被还原,错误;D、根据电荷守恒可知, x=4,正确。
本题难度:一般
2、选择题 【3分】硫代硫酸钠(Na2S2O3)可作为脱氯剂,已知25 mL 0.1 mol・L-1该溶液恰好把标准状况下的224 mL氯气完全还原,则产物中硫元素的化合价为(??? )
A.-2
B.0
C.+4
D.+6
参考答案:D
本题解析:Na2S2O3中,S为+2价,设其升高了x价。由电子得失守恒可得: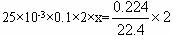
x=4故升高到+6价。
本题难度:简单
3、选择题 三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体,无色、无臭,在潮湿空气中泄露会产生白雾、红棕色气体等现象,反应方程式为:aNF3+bNF3=c?+dHNO3+eHF。下列说法正确的是
A.反应方程式横线处物质为NO,且a=3、b=5、c=2、d=1、e=9
B.反应中被氧化与被还原的原子物质的量之比为2:1
C.若反应中生成0.2molHNO3,则反应共转移0.2mole-
D.反应中NF3是氧化剂,H2O是还原剂
参考答案:A
本题解析:红棕色气体为NO2;根据氮元素化合价升降情况,反应不可能直接产生NO2,故反应方程式空格处物质为NO,配平反应方程式为3NF3+5NF3=2NO+HNO3+9HF
本题难度:一般
4、选择题 向27.2gCu和Cu2O的混合物中加入某浓度的稀硝酸0.5L,固体物质完全反应,生成NO和Cu(NO3)2,在所得溶液中加入1.0mol/L的NaOH溶液1.0L,此时溶液呈中性。金属离子已完全沉淀,沉淀质量为39.2g。下列有关说法不正确的是
A.Cu与Cu2O的物质的量之比为2∶1
B.硝酸的物质的量浓度为2.6mol/L
C.产生的NO在标准状况下的体积为4.48L
D.Cu、Cu2O与硝酸反应后剩余HNO3为0.2mol
参考答案:B
本题解析:设Cu和Cu2O的物质的量分别为xmol、ymol,根据题意,则有
64x+144y="27.2" ……①
由Cu Cu(OH)2? Cu2O
Cu(OH)2? Cu2O 本题难度:一般
本题难度:一般
5、选择题 将5.6 g Fe投入浓硝酸溶液中,产生红棕色气体A,把所得溶液蒸干,得到20g Fe(NO3)2和Fe(NO3)3的混合物,将该混合物在高温下加热,得到红褐色的Fe2O3和气体B,A、B气体混合通入水中,剩余气体的体积为:.
A.1120 mL??????B.2240 mL??????? C.360 mL????? D.4480 mL
参考答案:B
本题解析:
试题分析:利用整体思维抓住反应的始终态,根据题意反应物可看作Fe、HNO3和水,最终生成物是Fe2O3和剩余气体NO(剩余气体不可能是O2,违背电子得失守恒),在该过程中铁元素化合价由0价升高到+3价,氮元素的化合价由+5价降为+2价,根据电子守恒可得n(NO)=n(Fe),代入数据计算可得。
本题难度:一般