��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ij�жԴ������м��,���ָ�����Ҫ��Ⱦ��Ϊ�����������PM2.5(ֱ��С�ڵ���2.5��m������������),����Ҫ��ԴΪȼú��������β���ȡ����,��PM2.5��SO2��NOx�Ƚ����о�������Ҫ���塣
��ش���������:
(1)��PM2.5����������ˮ�����Ƴɴ���������
����ø���������ˮ���������ӵĻ�ѧ��ּ���ƽ��Ũ�����±�:
����
| K+
| Na+
| N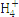
| S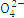
| N
| Cl-
|
Ũ��/mol��L-1
| 4��10-6
| 6��10-6
| 2��10-5
| 4��10-5
| 3��10-5
| 2��10-5
���ݱ��������ж�PM2.5�������Ϊ������������,������pH=������������������
(2)Ϊ����SO2���ŷ�,����ȡ�Ĵ�ʩ��:
�ٽ�úת��Ϊ�������ȼ�ϡ�
��֪:H2(g)+ O2(g) H2O(g) ��H="-241.8" kJ��mol-1 �� O2(g) H2O(g) ��H="-241.8" kJ��mol-1 ��
C(s)+ O2(g) CO(g)�� ��H="-110.5" kJ��mol-1 �� O2(g) CO(g)�� ��H="-110.5" kJ��mol-1 ��
д����̿��ˮ������Ӧ���Ȼ�ѧ����ʽ:�� ��
��ϴ�Ӻ�SO2���������������ʿ���ϴ�Ӽ�����������������������������
a.Ca(OH)2���� b.Na2CO3�� ��c.CaCl2�� ��d.NaHSO3
(3)����β����NOx��CO�����ɼ�ת��
����֪����������NO�ķ�ӦΪ:
N2(g)+O2(g) 2NO(g)����H>0 2NO(g)����H>0
��1 mol������0.8 mol N2��0.2 mol O2,1 300��ʱ���ܱ������ڷ�Ӧ�ﵽƽ��,���NOΪ8��10-4mol��������¶��µ�ƽ�ⳣ��K=������������������ ��
����������,�����¶�Խ��,��λʱ����NO�ŷ���Խ��,ԭ�������������������������������� ������
������ȼ�Ͳ���ȫȼ��ʱ����CO,�������밴���з�Ӧ��ȥCO:
2CO(g) 2C(s)+O2(g)
��֪�÷�Ӧ�Ħ�H>0,�����������ܷ�ʵ�ֵ�����:
��
��Ŀǰ,������β��ϵͳ��װ�ô�ת�����ɼ���CO��NO����Ⱦ,�仯ѧ��Ӧ����ʽΪ�� ��
�ο��𰸣���1������ 4
��
���������
�����������1�����ݵ���غ���ɵ�c��Cl-��+ c��NO3-��+2 c��SO42-��= c��K+��+ c��Na+��+c��NH4+��+ c��H+��������ɵ�c��H+��=1��10-4mol/L,pH="4," PM2.5�������Ϊ���ԣ�
��2���ٸ��ݸ�˹���ɿɵý�̿��ˮ������Ӧ���Ȼ�ѧ����ʽ=��-�٣����Դ���C(s)+ H2O(g)=CO(g)+H2(g) ��H=+131.3kJ/mol��
�ڶ�����������������ơ�̼������Һ��Ӧ���������Ȼ��ơ�������������Һ��Ӧ��������ϴ�Ӽ������������ơ�̼���ƣ���ѡab��
��3����N2(g)+O2(g) 2NO(g)��H>0����ʼʱ0.8 mol N2��0.2 mol O2,�ﵽƽ��, NOΪ8��10-4mol�����ݻ�ѧ����ʽ�ɼ����ƽ��ʱ���������������ʵ����ֱ�Ϊ0.7996mol��0.1996mol��NO��ϵ����2�����Ի�ѧƽ�ⳣ��K=c��NO��2/c(N2)c(O2)=n��NO��2/n(N2)n(O2)= (8��10-4mol)2/0.7996mol��0.1996mol=4��10-6���÷�Ӧ�����ȷ�Ӧ���¶�Խ�ߣ���Ӧ����Խ�죬������Ӧ������NO���ŷ���Խ�� 2NO(g)��H>0����ʼʱ0.8 mol N2��0.2 mol O2,�ﵽƽ��, NOΪ8��10-4mol�����ݻ�ѧ����ʽ�ɼ����ƽ��ʱ���������������ʵ����ֱ�Ϊ0.7996mol��0.1996mol��NO��ϵ����2�����Ի�ѧƽ�ⳣ��K=c��NO��2/c(N2)c(O2)=n��NO��2/n(N2)n(O2)= (8��10-4mol)2/0.7996mol��0.1996mol=4��10-6���÷�Ӧ�����ȷ�Ӧ���¶�Խ�ߣ���Ӧ����Խ�죬������Ӧ������NO���ŷ���Խ��
�ڴӷ���ʽ���жϣ��÷�Ӧ���������ؼ��ķ�Ӧ���κ��¶��¾����Է����У�
������β��ϵͳ��װ�ô�ת������Ŀ���ǰ��ж�����ת��Ϊ�����������̼�����������Ի�ѧ����ʽΪ2CO+2NO 2CO2+N2 2CO2+N2
���㣺�������غ���ɵ�Ӧ�ã���ҺpH�ļ��㣬��˹���ɵ�Ӧ�ã���ѧƽ�ⳣ���ļ��㣬��Ӧ�Է����жϣ���ѧ����ʽ����д
�����Ѷȣ�����
2��ѡ���� �йؼ������������
��ѧ��
| Si��O
| O=O
| Si��Si
| ����kJ��mol-1
| X
| 498��8
| 176
�������������ȼ�յ��Ȼ�ѧ����ʽ��Si��s��+O2��g��
�ο��𰸣�
���������
�����Ѷȣ�һ��
3��ѡ���� ���������У����й��ۼ������ӻ�������
A��NH3
B��HCl
C��NaOH
D��NaCl
�ο��𰸣�C
���������
���������һ����õĽ����ͻ��õķǽ��������γ����Ӽ����ǽ���Ԫ�ص�ԭ�Ӽ������γɹ��ۼ����������Ӽ��Ļ����������ӻ����ȫ���ɹ��ۼ��γɵĻ������ǹ��ۻ�����������Ȼ����ǹ��ۻ�������������Ǻ������Ӽ����ۼ������ӻ�����Ȼ����Ǻ������Ӽ������ӻ������ѡC��
�������������е��Ѷȵ����⣬��Ҫ�ǿ���ѧ���Ի�ѧ���Լ���ѧ���ͻ������ϵ����Ϥ�˽�̶ȣ����ڹ���ѧ���Ļ��������ѧ����Ӧ��������ѧϰЧ�ʡ���ȷ��ѧ���ͻ�����Ĺ�ϵ�Ǵ���Ĺؼ���
�����Ѷȣ�һ��
4��ѡ���� S����б����S�����������������ͬ�������塣
��֪���� S(��б��s)��O2(g) === SO2(g) ��H1����297.16 kJ��mol-1
�� S(������s)��O2(g) === SO2(g) ��H2����296.83 kJ��mol-1
�� S(���s) === S(������s) ��H3
����˵����ȷ���ǣ� ��
A����H3����0.33 kJ��mol-1
B�������������������������
C��S����б��s��===S��������s����H3��0��������ȵ�б���ȶ�
D��S����б��s��===S��������s����H3��0����б����������ȶ�
�ο��𰸣�A
������������ݸ�˹���ɿ�֪���٣��ڼ��õ��ۣ����ԡ�H3����297.16 kJ��mol-1��296.83 kJ��mol-1
����0.33 kJ��mol-1��A��ȷ����������Խ��Խ�ȶ�������������ȵ�б���ȶ���BCD���Ǵ���ģ���ѡA��
�����Ѷȣ���
5��ѡ���� �л����ڷ�Ӧ�У���������ԭ�Ӽ�Ĺ��ۼ�ȫ���ֶ��ѣ���C��H��C��C��C=C��C��O��C�TO�ȡ����и���Ӧ�У���Ӧ������ж��Ѽ������У���ȷ������ǣ�??��
��ѧ��Ӧ
| �Ҵ�����
| �Ҵ�����
| ��ȩ����
| ��֬����
| ����ˮ��
| A
| O��H
| C��H
| C��H
| C��O
| C��N
| B
| O��H
| O��H
| O��H
| C��O
| C��H
| C
| C��O
| C��O
| C��H
| C�TO
| C�TO
| D
| C��O
| C��H
| C��C
| C��O
| N��H
?
�ο��𰸣�A
��������������ѣ����⿼������ŵ����ʣ�����������ˮ���ǿ�����̣�������ʽ��ʾ��
R����OH + R�䣭OH ���� eq o(sup 0( EMBED PBrush ?R�� ��O R��+H2O
�Ҵ�����ʱ���Ҵ��ж��ѵļ���O��H������֬������ʵ������֬�ڼ��������·���ˮ�ⷴӦ�����ɸ�֬�����ƺ��ͣ����ѵļ���C��O��������ˮ��������ˮ�����ƣ�ֻ�Ƕ��ѵļ�����C��O��������C��N����
�Ҵ�����������ȩ�ǡ�ȥ�⡱���������ѵļ���O��H����C��H��:
 �����Ѷȣ�һ�� �����Ѷȣ�һ��
|
|
|
��վ�ͷ�QQ: 960335752 - 14613519 - 791315772