微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 1gCO2含有CO2分子a个,则阿伏加德罗常数的数值可表示为
A.22a
B.28a
C.44a
D.88a
参考答案:C
本题解析:分析:根据n=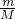 计算1gCO2的物质的量,再根据N=nNA计算阿伏加德罗常数,据此计算判断.
计算1gCO2的物质的量,再根据N=nNA计算阿伏加德罗常数,据此计算判断.
解答:1gCO2的物质的量为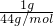 =
=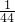 mol,
mol,
所以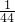 mol×NA=a
mol×NA=a
解得NA=44amol-1.
所以阿伏伽德罗常数的数值为44a.
故选:C
点评:考查阿伏伽德罗常数的计算,难度不大,注意公式运用及阿伏伽德罗常数的单位.
本题难度:简单
2、选择题 下列实验操作中正确的是( )
A.蒸馏实验中,温度计水银球应位于蒸馏烧瓶支管口处
B.制备乙酸乙酯的实验中,导管末端要伸入饱和Na2CO3溶液液面下
C.分液操作中,待下层液体流出后,再将上层液体从分液漏斗下口放出
D.测定溶液pH时,可用pH试纸蘸取少量待测液,并与标准比色卡比较
参考答案:A
本题解析:
本题难度:简单
3、填空题 (2008年北京卷,理综,27)(3)用图示装置制备NO并验证其还原性。有下列主要操作:
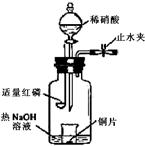
a.向广口瓶内注入足量热NaOH溶液,将盛有铜片的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸入瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中滴入少量稀硝酸。
①步骤c后还缺少的一步主要操作是___________________。
②红磷充分燃烧的产物与NaOH溶液反应的离子方程式是? ____________________________________________________________________。
③步骤c滴入稀硝酸后烧杯中的现象是_____________________________________
______________________________________________________________________。反应的离子方程式是____________________________________________________。
参考答案:(3)①打开止水夹,通入少量氧气;②P2O5+6OH-=2P
本题解析:以教材铜和稀硝酸反应实验设计为主体,用集气瓶、带有止水夹的导管巧妙地将两个部分连接起来,形成完整的、科学的实验设计。实验原理是利用红磷燃烧消除O2,再用铜和稀硝酸反应制备NO,观察现象:Cu片逐渐溶解,有无色气泡产生,溶液由无色变为蓝色,反应的离子方程式为:3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O;然后打开止水夹,让空气进入该装置,看到红棕色出现,发生了2NO+O2=2NO2,确定NO有还原性。故步骤c后还缺少的一步主要操作是打开止水夹,通入少量氧气。
本题难度:简单
4、选择题 已知乙烯能被酸性高锰酸钾溶液氧化成CO2。既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的少量乙烯的方法是(???)
A.在空气中燃烧
B.通入足量溴水中
C.通入酸性高锰酸钾溶液中
D.通入水中
参考答案:B
本题解析:燃烧不能除去乙烯,因为乙烷也能燃烧,A不正确。乙烷和酸性高锰酸钾溶液不反应,所以能鉴别乙烷和乙烯,但由于酸性高锰酸钾溶液能把乙烯氧化生成CO2,所以不能除去乙烷中的乙烯。乙烯和溴水发生加成反应,既能鉴别乙烷和乙烯,又能除去乙烷中的乙烯,B正确。乙烷和乙烯都不溶于水,D不正确,答案选B。
本题难度:简单
5、选择题 要除去KNO3溶液中混有的少量Ba(NO3)2杂质,得到纯净的KNO3溶液,操作正确的是( )
A.加入适量的Na2CO3溶液,过滤
B.加入足量的K2CO3溶液,过滤
C.先加入过量的K2CO3溶液,过滤,再向滤液中加入适量的稀HNO3
D.先加入过量的K2CO3溶液,过滤,再向滤液中加入适量的稀盐酸
参考答案:C
本题解析:
本题难度:一般