微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (12分)(1)要除去MgCl2酸性溶液里少量的Fe3+,可选用的试剂是 (填序号) 。
A.MgO
B.MgCO3
C.NaOH
D.Mg(OH)2
E.Fe(OH)3
(2)某温度下纯水中C(H+)=2×10-7 mol/L,则此时溶液中的C(OH-) = ;若温度不变,滴入稀盐酸使C(H+)=5×10-6 mol/L,则此时溶液中的C(OH-) = 。
(3)某温度下纯水的c(H+)=1.0×10-6 mol?L-1,在此温度下,将pH=8的Ba(OH)2与pH=5的稀盐酸混合,欲使pH=7,则Ba(OH) 2与稀盐酸的体积比为 。
参考答案:(1)ABD (2) 2×10-7 m
本题解析:
试题分析:(1)根据FeCl3的水解:FeCl3+3H2O Fe(OH)3+3HCl,加入MgO、Mg(OH)2、MgCO3均能促进FeCl3的水解,使其转化Fe(OH)3沉淀而除去,同时过量的MgO、Mg(OH)2、MgCO3可通过过滤除去,又不会引入新杂质。(2)纯水中 C(OH-) = C(H+) = 2×10-7 mol/L,Kw = C(H+)・C(OH-) = 2×10-7×2×10-7 = 4×10-14,稀盐酸中 C(OH-) ="Kw/" C(H+) = (4×10-14) / (5×10-6) = 8×10-9 mol/L。(3)纯水
Fe(OH)3+3HCl,加入MgO、Mg(OH)2、MgCO3均能促进FeCl3的水解,使其转化Fe(OH)3沉淀而除去,同时过量的MgO、Mg(OH)2、MgCO3可通过过滤除去,又不会引入新杂质。(2)纯水中 C(OH-) = C(H+) = 2×10-7 mol/L,Kw = C(H+)・C(OH-) = 2×10-7×2×10-7 = 4×10-14,稀盐酸中 C(OH-) ="Kw/" C(H+) = (4×10-14) / (5×10-6) = 8×10-9 mol/L。(3)纯水 说明,pH=6溶液呈中性,设Ba(OH)2溶液的体积为x,盐酸的体积为y,pH=8的Ba(OH)2溶液,c(OH-)=10-6mol/L,pH=5的盐酸,c(H+)=10-5mol/L,酸碱混合后,pH=7,则溶液呈碱性,反应剩余 c(OH-)="0.1" mol/L,则(10-6×x-10-5y)/( x+y) ="0.1" mol/L,解得x:y=2:9,
说明,pH=6溶液呈中性,设Ba(OH)2溶液的体积为x,盐酸的体积为y,pH=8的Ba(OH)2溶液,c(OH-)=10-6mol/L,pH=5的盐酸,c(H+)=10-5mol/L,酸碱混合后,pH=7,则溶液呈碱性,反应剩余 c(OH-)="0.1" mol/L,则(10-6×x-10-5y)/( x+y) ="0.1" mol/L,解得x:y=2:9,
考点:考查物质的分离提纯,酸碱混合时的定性判断及有关ph的计算。
本题难度:一般
2、选择题 下列过程或现象与盐类水解无关的是
A.纯碱溶液去油污
B.粗盐在空气中易潮解
C.加热氯化铁溶液颜色变深
D.浓硫化钠溶液有臭味
参考答案:B
本题解析:
试题分析: A.纯碱水解使溶液显碱性,有利于油脂的水解去除油污,与盐类水解有关,A不选;B.粗盐中含有氯化镁,氯化镁易潮解导致粗盐易潮解,与盐类水解无关,B选;C.溶液颜色变深是因为加热促进盐类水解,C不选;D.溶液有臭味是因为硫化钠水解后产生了少量有臭味的硫化氢,D不选;答案选B。
考点:考查盐类水解的应用。
本题难度:一般
3、选择题 有物质的量浓度、体积都相同的NaF溶液和NaCN溶液.已知HF比HCN较易电离.则溶液中离子总数的关系正确的是
A.NaF=NaCN
B.NaF>NaCN
C.NaFD.无法确定
参考答案:B
本题解析:
本题难度:一般
4、填空题 现有浓度均为0.1mol・L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④氯化铵、⑤醋酸铵、⑥硫酸氢铵、⑦氨水,请回答下列问题:
(1)①、②、③、④四种溶液中由水电离出的H+浓度由大到小的顺序是(填序号)____________。
(2)④、⑤、⑥、⑦四种溶液中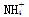 浓度由大到小的顺序是(填序号)________。
浓度由大到小的顺序是(填序号)________。
(3)将③和④按体积比1
参考答案:
本题解析:
本题难度:一般
5、选择题 物质的量浓度相同的下列溶液中,含粒子种类最多的是
A.CaCl2
B.CH3COONa
C.NH3
D.K2S
参考答案:D
本题解析:
试题分析:CaCl2不水解,溶液中存在的粒子有Ca2+、Cl-、OH-、H+、H2O 5种;CH3COONa发生水解,溶液中存在Na+、CH3COO-、CH3COOH、H+、OH-、H2O 6种粒子;氨水中存在NH3、NH3・H2O、NH4+、OH-、H+、H2O 6种粒子;K2S中S2-发生两步水解,溶液中存在K+、S2-、HS-、H2S、OH-、H+、H2O 7种粒子 ,答案选D。
考点:考查盐类的水解和水的电离。
本题难度:简单