��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��4�֣�������NH4I�����ܱ������У�ij�¶��·������б仯��
NH4I(s) 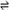 ?NH3 (g) + HI(g)??????? 2HI(g)
?NH3 (g) + HI(g)??????? 2HI(g) 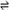 ?H2(g) + I2(g)
?H2(g) + I2(g)
����Ӧ�ﵽƽ��ʱc (H2)=" 0.5" mol/L, c (HI)=" 4" mol/L, �� c��NH3��??????��HI ��
�ֽ���Ϊ???????��
2��ѡ���� ��֪NO2��N2O4�����ת����2NO2(g)  N2O4(g)? ��H��0���ֽ�һ����NO2��N2O4�Ļ������ͨ��һ���Ϊ1 L�ĺ����ܱ������У���Ӧ��Ũ����ʱ��仯��ϵ����ͼ��ʾ��X��Y���������У�Y��ʾN2O4Ũ����ʱ��ı仯��������˵������ȷ����
N2O4(g)? ��H��0���ֽ�һ����NO2��N2O4�Ļ������ͨ��һ���Ϊ1 L�ĺ����ܱ������У���Ӧ��Ũ����ʱ��仯��ϵ����ͼ��ʾ��X��Y���������У�Y��ʾN2O4Ũ����ʱ��ı仯��������˵������ȷ����
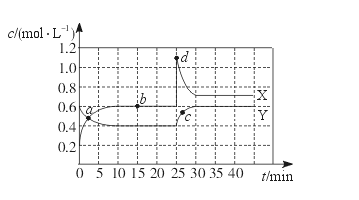
A�����������ѹǿ���䣬˵����Ӧ�Ѵﻯѧƽ��״̬
B��a��b��c��d�ĸ����У���ʾ��ѧ��Ӧ����ƽ��״̬�ĵ���b��
C��25��30 min����NO2��ʾ��ƽ����ѧ��Ӧ������0.08 mol��L��1��min��1
D����Ӧ������25 minʱ�����߷����仯��ԭ��������N2O4Ũ��
3��ѡ���� �����£����ݻ�Ϊ2L���ܱ������з���3A��g��+2B��g�� ? 2C��g��+xD (s)��Ӧ������ʼͶ��Ϊ3molA��2molB��2min��ƽ�⣬����D1.2mol����ôӷ�Ӧ��ʼ��ƽ��C������Ϊ0.3mol(L��min)�����н��۲���ȷ����
? 2C��g��+xD (s)��Ӧ������ʼͶ��Ϊ3molA��2molB��2min��ƽ�⣬����D1.2mol����ôӷ�Ӧ��ʼ��ƽ��C������Ϊ0.3mol(L��min)�����н��۲���ȷ����
A.x="2????????????????????????????????????????"
B.ƽ��ʱ��c(A)=0.6mol/L
C.ƽ��ʱ��C���������Ϊ37.5��
D.��n(A) : n(B) : n(C) : n(D)="3" : 2 : 3 : 3����Ͷ�ϣ�ƽ�ⲻ��
4��ѡ���� ij�¶��£� ��ƽ�ⳣ��K=9/4�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�����±� ��ʾ��
��ƽ�ⳣ��K=9/4�����¶����ڼס��ҡ������������ܱ������У�Ͷ��H2(g)��CO2(g)������ʼŨ�����±� ��ʾ��
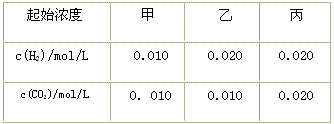 ? ?
�����жϲ���ȷ���� [???? ]
A��ƽ��ʱ������CO2��ת���ʴ���60%
B��ƽ��ʱ�����кͱ���H2��ת���ʾ���60%
C��ƽ��ʱ������c(CO2)�Ǽ��е�2������0.012 mol/L
D����Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
5������� (14��)��2011��11��28����12��9�գ����Ϲ�����仯��ܹ�Լ��17�ε�Լ���������Ϸǵ°��ٿ����������������ЧӦ����Դ��ȱ����������ӣ���ν��ʹ�����CO2�ĺ�������Ч�ؿ�������CO2�������˸������ձ����ӡ�
��1��Ŀǰ��ҵ����һ�ַ�������CO2������ȼ�ϼ״���Ϊ̽���÷�Ӧԭ������������ʵ�飬�����Ϊ1L���ܱ������У�����1mol CO2��3.25 mol H2����һ�������·�����Ӧ���ⶨCO2��CH3OH(g)��H2O (g)��Ũ����ʱ��仯��ͼ��ʾ��
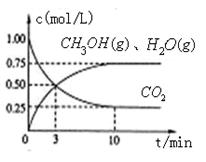
��д���ù�ҵ������ȡ�״��Ļ�ѧ��Ӧ����ʽ������������������
�ڴӷ�Ӧ��ʼ��ƽ�⣬������ƽ����Ӧ����v (H2)����??????? �� ��
�۸�������CO2��ת����Ϊ��??????????????�����¶Ƚ���ʱCO2��ת���ʱ����÷�Ӧ???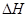 ??����������������������� ??�����������������������
�����д�ʩ����ʹn(CH3OH)/n(CO2)�����������������������
A�������¶�
B�����뵪��
C����ˮ��������ϵ�з���
D���ø���Ч�Ĵ���
��2��ѡ�ú��ʵĺϽ���Ϊ�缫�����������ơ��״���ˮ������Ϊԭ�ϣ������Ƴ�һ���Լ״�Ϊԭ�ϵ�ȼ�ϵ�أ���ȼ�ϵ�ظ����ĵ缫����ʽΪ������������������������
���о�NO2 ?��SO2 ��CO�ȴ�����Ⱦ����Ĵ���������Ҫ���塣���е�Ԫ�����Ŷ���̬�������Ļ���������ڹ�ũҵ�����������з�������Ҫ�����á�����������⣺
��1����֪��2SO2(g) + O2(g) 2SO3(g)? ��H=" ��196.6" kJ��mol�D1 2SO3(g)? ��H=" ��196.6" kJ��mol�D1
2NO(g) + O2(g) 2NO2(g)? ��H= ��113.0 kJ��mol�D1 2NO2(g)? ��H= ��113.0 kJ��mol�D1
��ӦNO2(g) + SO2(g) SO3(g) + NO(g) �Ħ�H= ???????????????????????�� SO3(g) + NO(g) �Ħ�H= ???????????????????????��
��2��һ�������£���NO2��SO2�������1:2�����ܱ������з���������Ӧ��
��������˵����Ӧ�ﵽƽ��״̬����?????????????(�����) ��
a����ϵѹǿ���ֲ���?????????????? b�����������ɫ���ֲ���
c��SO3��NO������ȱ��ֲ���????? d����ͬʱ���ڣ�ÿ����1 molNO2��ͬʱ����1 mol SO3
�ڵ����������Ӧƽ��ʱNO2��SO2�����Ϊ1: 6����ƽ�ⳣ��K��???????????��
|