微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 实验室里若用下图装置制取氨气,请指出图中存在的问题,并简要说明如何改正。
存在问题:
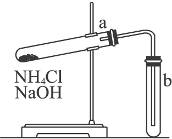
改正方法:
参考答案:错误之处:①所用试剂,②试管a的管口方向,③试管b管口向上,
本题解析:判断气体实验装置是否有错误,一般主要看:发生装置、试剂使用、实验原理、收集方法、实验安全(如尾气处理,是否引起爆炸、飞溅等)五方面是否有误。
本题难度:简单
2、选择题
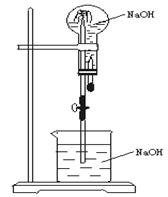
A.HCl和CO2
B.NH3和CH4
C.SO2和CO
D.NO和NO2
参考答案:A
本题解析:应选择极易与NaOH反应(或说极易被NaOH吸收)的物质。其中只有A符合。B中的CH4,C中的CO,D中的NO本身都不与NaOH反应,故不选。
注:如是混合气,则NO2与NO又为等摩尔混合时也可进行喷泉实验。因NO2+NO+2NaOH===2NaNO2+H2O。
本题难度:简单
3、选择题 在某稀硝酸的溶液中,加入5.6g铁粉充分反应后,铁粉全部溶解,放出NO气体,溶液质量增加3.2g,所得溶液中Fe2+和Fe3+物质的量之比为(??)
A.1:1
B.3:2
C.2:1
D.4:1
参考答案:B
本题解析:设生成的NO的质量为5.6―3.2=2.4g,物质的量为 =0.08mol
=0.08mol
设溶液中Fe2+和Fe3+物质的量分别为a、b
两者的总物质的量为a+b= 本题难度:一般
本题难度:一般
4、填空题 (12分)Ⅰ、氮元素的氢化物和氧化物在工业生产和国防建设中都有广泛应用。回答下列问题:(1)氮元素原子的L层电子数为__________;
(2) NH3与NaClO反应可得到肼(N2H4),该反应的化学方程式为_________________________;
(3) 肼-空气燃料电池是一种碱性电池,该电池放电时,正极的反应式为________________________________。
Ⅱ、一定质量的液态化合物XY2在标准状况下的一定质量的O2中恰好完全燃烧,反应方程式为: XY2(l)+3O2 (g) ="==" XO2(g)+2YO2 (g)冷却后,在标准状况下测得生成物的体积是672 mL,密度是2.56g/L则: (1)反应前O2的体积是________。(2)化合物XY2的摩尔质量是___________。
(3)XY2分子中X、Y两元素质量比是3∶16, X、Y两元素分别为__________ (写元素符号)。
参考答案:、12分) (每空2分)
Ⅰ (1)5??? (2)2
本题解析:Ⅰ (1)根据原子核外电子的排布规律可知,氮元素原子的L层电子数为5个。
(2)根据原子守恒可知,还有氯化钠和水生成,所以反应的方程式是
2NH3+NaClO=N2H4+NaCl+H2O。
(3)原电池中分解失去电子,正极得到电子,所以正极是氧气得到电子。电解质溶液显碱性,所以正极电极反应式是O2+2H2O +4e-=4OH-。
Ⅱ、(1)根据反应的方程式可知,反应前后体积是不变的,所以反应前氧气的体积是672ml。
(2)氧气的物质的量是0.03mol,质量是0.96g。反
本题难度:一般
5、选择题 将盛有12mLNO2和O2混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积和剩余的气体分别是???( ????)
A.2.4 mL、O2
B.1.2mL、NO
C.4 mL、O2
D.3.6 mL、NO
参考答案:BC
本题解析:NO2和O2混合气通入水中的反应:4 NO2 +O2+2H2O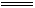 4HNO3。剩余2mL无色气体可能是NO或O2。如是O2,则溶于水的气体为10mL,其中O2为2mL,NO2为8mL,即原混合气体中含NO2为8mL,O2为4mL。如是NO,则溶于水的气体为6mL,其中O2为1.2mL,N O2为4.8mL,即原混合
4HNO3。剩余2mL无色气体可能是NO或O2。如是O2,则溶于水的气体为10mL,其中O2为2mL,NO2为8mL,即原混合气体中含NO2为8mL,O2为4mL。如是NO,则溶于水的气体为6mL,其中O2为1.2mL,N O2为4.8mL,即原混合
本题难度:一般