微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 乙醇(C2H6O)水溶液中,当乙醇分子和水分子中氢原子个数相等时,溶液中乙醇的质量分数为(?)
A.20%
B.50%
C.46%
D.32%
参考答案:C
本题解析:
试题分析:乙醇分子和水分子中氢原子个数相等,则H原子物质的量相等,设H原子为nmol,则乙醇的质量分数为=nmol÷6×46g/mol÷(nmol÷6×46g/mol+nmol÷2×18g/mol)×100%=46%,故C项正确。
本题难度:一般
2、选择题 在相同温度下,在体积相同的两个密闭容器内充入等质量的CO2和SO2气体,则下列说法正确的是
A.CO2和SO2中物质的量比为 1:1
B.CO2和SO2的密度比为1:1
C.CO2和SO2的物质的量浓度比为11:16
D.CO2和SO2中所含氧原子个数比为16:11
参考答案:BD
本题解析:
试题分析:等质量的CO2和SO2气体的物质的量之比是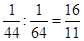 。所以根据阿伏加德罗定律及其推论可知,A不正确,CO2和SO2中物质的量比为 16:11, B正确;C不正确,CO2和SO2的物质的量浓度比为16:11;二者都含有2个氧原子,D正确,答案选BD。
。所以根据阿伏加德罗定律及其推论可知,A不正确,CO2和SO2中物质的量比为 16:11, B正确;C不正确,CO2和SO2的物质的量浓度比为16:11;二者都含有2个氧原子,D正确,答案选BD。
点评:该题是高考中的常见题型和重要的考点,属于中
本题难度:简单
3、填空题 (10分)(1)实验室里常用浓盐酸与二氧化锰反应来制取少量的氯气,反应的化学方程式为:MnO2+4HCl(浓)  MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
MnCl2+Cl2↑+2H2O,取一定量的浓盐酸使其与二氧化锰发生反应,产生的氯气在标准状况下的体积为22.4 L。
请回答下列问题:
①写出该反应的离子反应方程式_________________________,②反应中被氧化的HCl的物质的量为 ________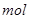 。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g・cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________
。③实验室备用的浓盐酸质量分数为36.5%,密度为1.19 g・cm-3,为使用方便,请计算出该浓盐酸的物质的量浓度_________ 。
。
(2)把一小块镁铝合金溶于100mL盐酸中,然后向其中滴入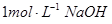 溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。
溶液,生成沉淀的质量和加入NaOH溶液的体积如下图所示。

①合金中镁的质量 g。
②盐酸的物质的量浓度  。
。
参考答案:①MnO2+2Cl-+4H+===Mn2++Cl2↑+2H2
本题解析:
试题分析:本题涉及Cl2的实验室制法,难度不大。结合图像的计算也属基础题型,关键结合题给信息,分析图中的数据再根据方程式计算可得。10mLNaOH用于中和盐酸,40mLNaOH用于沉淀Mg2+ 、Al3+;Cl-转化为NaCl,由Na+可确定Cl-的量,即HCl的物质的量,为0.05mol;可求得盐酸的浓度为0.5mol/L;结合图像B C发生反应Al(OH)3+OH-=AlO2-+2H2O,计算消耗NaOH的物质的量为0.01mol,可知用于沉淀Al3+的OH-为0.03mol,则其余用于沉淀Mg2+,由反应Mg2++2OH-=Mg(OH)2↓可求得Mg2+的物质的量为0.005mol,从而金属Mg的质量为0.12g。
C发生反应Al(OH)3+OH-=AlO2-+2H2O,计算消耗NaOH的物质的量为0.01mol,可知用于沉淀Al3+的OH-为0.03mol,则其余用于沉淀Mg2+,由反应Mg2++2OH-=Mg(OH)2↓可求得Mg2+的物质的量为0.005mol,从而金属Mg的质量为0.12g。
考点:化学计算。
本题难度:一般
4、选择题 在一定温度下,已知有关某溶液的一些数据:①溶液的质量?②溶剂的质量 ③溶液的体积 ④溶质的摩尔质量 ⑤溶质(气体)的体积(Vm已知) ⑥溶液的密度 ⑦溶液的质量分数。利用下列各组数据计算该溶液的物质的量浓度,不能算出的一组是
A.③⑤
B.②④⑤⑥
C.①④⑥
D.①②③④
参考答案:C
本题解析:本题考查物质的量与溶质质量分数之间的相互换算关系。计算物质的量浓度公式有:c=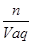 =
=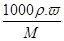 ,C项缺溶质质量,不能计算物质的量
,C项缺溶质质量,不能计算物质的量
本题难度:一般
5、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是
A.500 mL 2 mol・L-1 FeCl3溶液中Fe3+数为NA,且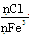 =3
=3
B.1 L pH=1的硫酸溶液中含有的H+为0.2NA
C.标准状况下,22.4L 乙烷中含极性共价键的数目为7NA
D.12 g石墨和C60的混合物中质子总数一定为6NA个
参考答案:D
本题解析:
试题分析:A、氯化铁溶液中,铁离子发生水解,使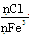 >3,错误;B、pH=1的溶液中氢离子的浓度是0.1mol/L,则1L溶液中氢离子的物质的量是0.1mol,数目是0.1NA,错误;C、标准状况下,22.4L乙烷的物质的量是1mol,1个乙烷分子中含有6个极性共价键,所以标准状况下,22.4L 乙烷中含极性共价键的数目为6NA,错误;D、石墨和C60都是C元素的单质,构成原子都是C原子,所以12 g石墨和C60的混合物中C原子的物质的量是1mol,1个C原子中含有个质子,所以质子总数一定为6NA个,正确,答案选D。
>3,错误;B、pH=1的溶液中氢离子的浓度是0.1mol/L,则1L溶液中氢离子的物质的量是0.1mol,数目是0.1NA,错误;C、标准状况下,22.4L乙烷的物质的量是1mol,1个乙烷分子中含有6个极性共价键,所以标准状况下,22.4L 乙烷中含极性共价键的数目为6NA,错误;D、石墨和C60都是C元素的单质,构成原子都是C原子,所以12 g石墨和C60的混合物中C原子的物质的量是1mol,1个C原子中含有个质子,所以质子总数一定为6NA个,正确,答案选D。
考点:考查阿伏伽德罗常数与微粒数、化学键数的关系
本题难度:一般