微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 据报道,氢燃料电池公交汽车已经驶上北京街头.下列说法正确的是( )
A.电解水制取氢气是理想而经济的制氢方法
B.发展氢燃料电池汽车不需要安全高效的储氢技术
C.氢燃料电池把氢气和氧气燃烧放出的热能转化为电能
D.氢燃料电池汽车的使用可以有效减少城市空气污染
参考答案:A、电解水制取氢气消耗大量的电能,电解水制取氢气是理想而经济
本题解析:
本题难度:简单
2、选择题 (2014届上海市十三校高三测试化学试卷)
2013年12月31日夜,上海外滩运用LED产品进行了精彩纷呈的跨年灯光秀。下图是一种氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是???
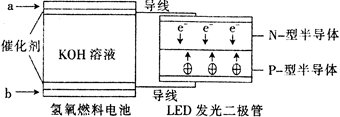
A.a处通入氧气
B.b处为电池正极,发生了还原反应
C.该装置中只涉及两种形式的能量转化
D.P-型半导体连接的是电池负极
参考答案:B
本题解析:
由于电子从在LED发光二极管的N极向P极移动,所以N极与电源的负极连接,P极与电源的正极连接。所以在燃料电池中a处通入的气体为氢气,该处为负极,发生氧化反应;在b处通入的气体为氧气,该处为正极,发生还原反应。在该装置中涉及的能量转化形式有化学能转化为电能,以及电能转化为光能及热能。所以正确选项为B。
本题难度:一般
3、填空题 有甲、乙两位同学均想利用原电池反应检测金属的活动性顺序,两人均使用镁片与铝片作电极,但甲同学将电极放入6 mol・L-1 H2SO4溶液中,乙同学将电极放入6 mol・L-1的NaOH溶液中,如图所示。
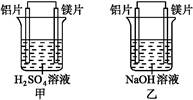
请回答:
(1)写出甲池中正极的电极反应式: 。
(2)写出乙池中负极的电极反应式和总反应的离子方程式:负极 ,总反应的离子方程式为 。
(3)如果甲、乙同学均认为“构成原电池的电极材料如果都是金属,则构成负极材料的金属应比构成正极材料的金属活泼”,则甲会判断出 活动性更强,而乙会判断出 活动性更强(填写元素符号)。
(4)由此实验,可得到如下哪些正确结论? (填写字母序号)。
a.利用原电池反应判断金属活动性顺序时应注意选择合适的介质
b.镁的金属性不一定比铝的金属性强
c.该实验说明金属活动性顺序已过时,已没有实用价值
d.该实验说明化学研究对象复杂,反应受条件影响较大,因此应具体问题具体分析
(5)上述实验也反过来证明了“直接利用金属活动性顺序判断原电池中的正负极”,这种做法 (填“可靠”或“不可靠”)。
参考答案:
(1)2H++2e- 本题解析:
本题解析:
试题分析::原电池的负极是相对活泼的金属,因金属活动性顺序的排列是在一般酸中的反应顺序。那么,当溶液改为NaOH溶液时,由于Mg不反应,而Al能跟NaOH溶液反应,在这种情况下,对于NaOH溶液而言,Al比Mg活泼,在该装置中铝作负极。因此,判断原电池正负极时,应考虑到对应介质,谁更易跟电解质溶液反应,谁就作负极。
考点:原电池、电解池、电镀
本题难度:一般
4、选择题 判断在下列装置中电流表能发生偏转的是( )
A.
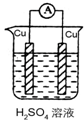
B.
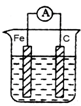
C.
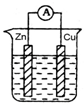
D.
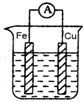
参考答案:A、两电极材料相同,且电极材料和电解质溶液不发生氧化还原反应
本题解析:
本题难度:一般
5、选择题 某原电池工作时总的反应为Zn+Cu2+===Zn2++Cu,该原电池的组成可能是??
A.Zn为正极,Cu为负极,CuCl2溶液作电解质溶液
B.Cu为正极,Zn为负极,稀H2SO4作电解质溶液
C.Cu为正极,Zn为负极,CuSO4溶液作电解质溶液
D.Fe为正极,Zn为负极,CuCl2溶液作电解质溶液
参考答案:CD
本题解析:把电池反应方程式拆成两个半电池,发生氧化反应的电极为负极,所以锌作负极;发生还原反应的电极为正极,所以用不如锌活泼的金属或非金属导体作正极;含有发生还原反应的离子溶液为电解质溶液,所以是含有铜离子的溶液.
故选CD.
本题难度:一般