��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� �ȼ��ⱥ��ʳ��ˮ��ȡNaOH�Ĺ�������ʾ��ͼ���£�
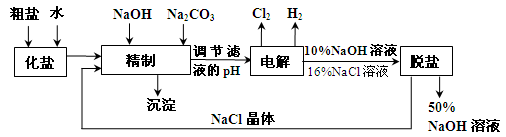
������ͼ����������⣺
�ڵ������У���������������ĵ���ʽΪ?????��
��2�����ƹ����г�ȥ�������е�Ca2+��Mg2+�����ʣ���ȥMg2+�����ӷ���ʽΪ????��
��3�����ƹ���Ҫ��ȥ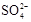 ����ѡ��������Һ�е�???������ĸ��ţ������������˳���Լ�ͷ���ţ���������ʽ����ͼ�ϣ����ƹ����м����Լ������ҵ�˳��Ϊ�Ⱥ�˳��
����ѡ��������Һ�е�???������ĸ��ţ������������˳���Լ�ͷ���ţ���������ʽ����ͼ�ϣ����ƹ����м����Լ������ҵ�˳��Ϊ�Ⱥ�˳��
a.Ba(OH)2?????????? b.Ba(NO3)2????????? c.BaCl2
��4����ʵ��������Ҳ������BaCO3��ȥ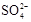 ����֪�ܽ��BaSO4��BaCO3)������ƽ���ƶ�ԭ�����Խ��ͣ�?????��
����֪�ܽ��BaSO4��BaCO3)������ƽ���ƶ�ԭ�����Խ��ͣ�?????��
��5�����ι����У�����NaOH��NaCl���ܽ���ϵIJ��죬ͨ����������ȴ��???������������ƣ����Ƶ�50%��NaOH��Һ��
2��ѡ���� �Ӵ���������ͨ����400��500�桢��ѹ�ʹ����������£���SO2�������O2��Ӧ����SO3��2SO2(g)��O2(g) 2SO3(g)?��H��0�������������£�SO2��ת����ԼΪ90%�����Dz��ַ�����Ҳ��ø�ѹ�������SO3 ����ȡ��ѹ��ʩ��Ŀ��
2SO3(g)?��H��0�������������£�SO2��ת����ԼΪ90%�����Dz��ַ�����Ҳ��ø�ѹ�������SO3 ����ȡ��ѹ��ʩ��Ŀ��
A��������ҵ��ܹ������Դ����Ĵ�����Դ
B����ѹ��ʹƽ��������Ӧ�����ƶ��������ڽ�һ�����SO2��ת����
C����ѹ��ʹSO2ȫ��ת��ΪSO3 ������SO2�Կ�������Ⱦ
D����ѹ�����ڼӿ췴Ӧ���ʣ��������Ч��
3������� ��14�֣�þ���仯��������������������Ҫ�����á���ˮ��þʯ(��Ҫ�ɷ�ΪMgCl2��6H2O)Ϊԭ��������ʽ̼��þ����Ҫ�������£�

��1�����������е���ҺŨ���ᾧ��������Ҫ�������ʵĻ�ѧʽΪ???????????��ָ���������ڹ�ũҵ�����е�һ����;��???????????��
��2��д��Ԥ����ʱ��������Ҫ��Ӧ�����ӷ���ʽ��?????????????????????????��
��3������þʱ��Ӧ���¶Ȳ��˹��ߣ�ԭ����???????????????????????????��
��4�����һ��ʵ�飬ȷ����Ʒ��ʽ̼��þaMgCO3��bMg(OH)2��cH2O��a��b��c��ֵ������������ʵ�鲽�裨�����Լ���Ũ���ᡢ��ʯ�ң���
����Ʒ�������ڸ��·ֽ⣻��???????????????����??????????????���ݳ���MgO��
18.2g��Ʒ��ȫ�ֽ����6.6g CO2��8.0g MgO���ɴ˿�֪����Ʒ�Ļ�ѧʽ�У�
a=????????��b =????????��c =????????��
��5����ˮ��þʯ�п�����ȡ��ˮ�Ȼ�þ���������̬����ˮ�Ȼ�þ���Եõ�����þ����ͬѧ��Ϊ��������ڵ�MgOҲ���ƽ���þ����ʵ�������пɼ��������裬���������ļ�Լ�Ժ;�����ԭ����ͬ���ͬѧ���뷨��Ϊʲô����Ĺ۵���??????????????????????��������?????????????????????????????????????????????????????????????????��
4������� ( 16�֣�����ZnO�׳�п1-3���ܸ��J�����Ļ�ѧ�ȶ��ԣ��������������ֲ���,���ij�������������䣬��Ϳ�ϡ�����ȹ�ҵҲ����ҪӦ�á���ҵ���ɴ�ZnO(��FeO��CuO��.)�Ʊ�����ZnO,��ȡ������������ӡ��кͳ������������յȲ��裬������������:
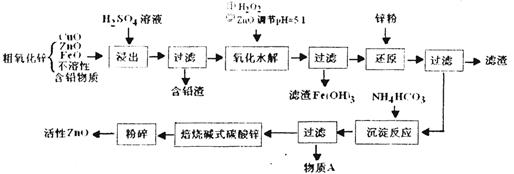
(1 )����������,�����õ���60%H2SO4(1.5g/cm3)��������������ʵ���Ũ��Ϊ________(������λС��)
(2 )��֪ZnOΪ���������������������Һ��Ӧ���ɿ����Ե�п����(Zn02-)��д����Ӧ�����ӷ���ʽ________________
(3) д����H2O2��������Ӧ�����ӷ���ʽ________________
(4) ��ȥFe(OH)3��,����Һ�м���Zn��Ŀ����________
(5) ���������ж�ν����˹��˙]������д������ʱ�õ��IJ���������________________
(6) ����A��________,��������������ӵķ�����________
(7) ȡ��ʽ̼��п6.82g��������������C02 448mL(��״���£����ܽ��������HCl 0. 12mol,���ü�ʽ������Ԫ�ص���������Ϊ1.76%�����Ʋ�ü�ʽ̼��п�Ļ�ѧʽ________
5��ѡ���� ����ʵ�����̷��ϻ�ѧʵ�顰��ɫ����ԭ����ǣ�������
A����ͭ�۴���ͭ˿����ͭ��Ũ���ᷴӦ��ʵ��
B����˫��ˮ������������ȡ����
C����ϩ�ۺ�Ϊ����ϩ�߷��Ӳ���
D���ö�����������������ʵ��