微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列各组液体混合物,能用分液漏斗分离的是( )
A.乙酸和水
B.溴苯和苯
C.己烷和水
D.乙醇和水
参考答案:A、乙酸和水互溶,不能用分液漏斗进行分离,故A错误;
本题解析:
本题难度:简单
2、选择题 下列现象或事实可用同一化学原理来解释的是( )
A.氯化铵和碘都可以用加热法进行提纯
B.氯水和二氧化硫气体均能使品红溶液退色
C.硫酸亚铁溶液和氢氧化钠溶液在空气中久置后均会变质
D.铁片和铝片置于冷的浓硫酸中均无明显现象
参考答案:A.氯化铵加热分解、碘加热升华,所以不能用加热法进行提纯,故
本题解析:
本题难度:一般
3、填空题 (10分)实验室有三瓶失去标签的无色溶液:氯化钾、氢氧化钙和稀硫酸,可用一种常见酸碱指示剂X 或Na2CO3一次鉴别它们。根据有关操作及所加试剂填空。
 ??????????
?????????? ????????
????????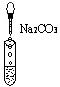
A??????????????? B????????????? C
(1)A试管中的现象:溶液显紫色;另取该溶液滴入Na2CO3溶液中,无明显现象。
试推断试剂X为????????。
(2)B试管中的现象:溶液显蓝色;另取该溶液滴入Na2CO3溶液中的现象为???????? ___
有关反应的离子方程式为???????? __________。
(3)C试管中的现象:有气泡产生,有关反应的离子方程式为???????????? _________;???
另取该溶液滴入试剂X, 则溶液显 _____________。
参考答案:(每空2分,共10分)(1)紫色石蕊试液
(2)有白
本题解析:
试题分析:(1)氯化钾是盐,溶液显中性,氢氧化钙是强碱,硫酸是强酸。根据酸碱指示剂的变色可知,A中溶液显紫色,这说明X一定是紫色的石蕊试液,因此A中的溶液一定不是硫酸。又因为另取该溶液滴入Na2CO3溶液中,无明显现象,所以该溶液是氯化钾。
(2)碱能使紫色的石蕊试液显蓝色,所以B中溶质是氢氧化钙,则滴入Na2CO3溶液中的现象为有白色沉淀生成,反应的离子方程式是CO32-+Ca2+=CaCO3↓。
(3)C中是硫酸。硫酸和碳酸钠反应生成CO2气体,反应的离子方程式CO32-+2H+=H2O+CO2↑;酸能使紫色的石蕊试液显红色。
点评:该题是高考中的常见题型,试题基础性强,难易适中。该题的突破点是溶液显紫色,然后再依据有关物质的化学性质,逐一分析、排除即可得出正确的结论。该题有利于培养稀释的逻辑思维能力和发散思维能力。
本题难度:一般
4、实验题 海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是________(填序号)
A.Cl2
B.淡水
C.烧碱
D.食盐
(2)从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是________________________。
(3)下图是从海水中提取镁的简单流程。
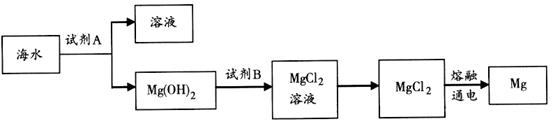
①工业上常用于沉淀Mg2+的试剂A是________,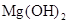 转化为MgCl2的离子方程式是________________________________。
转化为MgCl2的离子方程式是________________________________。
②由无水MgCl2制取Mg的化学方程式是________________________。
(4)海带灰中富含以I-形式存在的碘元素。实验室提取I2的途径如下所示:
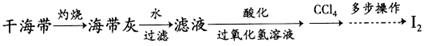
①灼烧海带至灰烬时所用的主要仪器名称是________________。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式____________________________。
反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈________色。
参考答案:(1)BD(2)Cl2 + 2Br- = 2Cl- + Br
本题解析:
试题分析:(1)海水蒸发可以得到淡水,并且可析出氯化钠,均为物理变化。
(2)Cl2 + 2Br- = 2Cl- + Br2 ?
(3)可用可溶性碱与镁离子反应生成 Mg(OH)2 沉淀。Mg(OH)2 + 2H+ = Mg2+ + 2H2O???? MgCl2(熔融) Mg+Cl2↑
Mg+Cl2↑
(4)①坩埚 可以直接在酒精灯上加热的仪器有试管、圆底烧瓶、蒸发皿、坩埚。坩埚可以加强热。
②2I- + H2O2 + 2H+ = I2 + 2H2O
③ 紫色,碘被萃取。
本题难度:一般
5、选择题 用下列实验装置进行相应实验,能达到实验目的是( )

A.用图(a)所示装置除去Cl2中含有的少量HCl
B.用图(b)所示装置蒸干NH4Cl饱和溶液制备NH4Cl晶体
C.用图(c)所示装置制取少量纯净的CO2气体
D.用图(d)所示装置分离CCl4萃取碘水后已分层的有机层和水层
参考答案:D
本题解析:
本题难度:一般