微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 化学学习小组对某镁铝合金进行了如下实验研究,请你参与并完成对有关问题的解答.
实验药品:9.0g镁铝合金,100mLamol/L稀硫酸,260mL5mol/L氢氧化钠溶液.
实验步骤
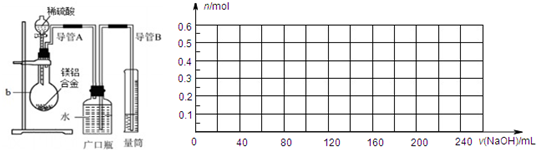
①将9.0g镁铝合金与100mLamol/L稀硫酸在图所示装置中充分反应至反应完毕,并收集生成的全部气体.
②向b内的混合液中逐滴加入260mL5mol/L氢氧化钠溶液并充分混合,当氢氧化钠溶液滴加至200mL时生成的沉淀量最大.
问题讨论
(1)仪器b的名称是______.
(2)根据实验目的可知,9.0g镁铝合金与100amol/L稀硫酸反应时,应该过(足)量的物质是______(填“镁铝合金”或“稀硫酸”),以保证另一种物质能够完全反应无剩余.
(3)实验步骤②中,当b内混合液中因滴加氢氧化钠溶液至生成的沉淀量最大时,此时所得溶液中的溶质是______.
(4)实验步骤①结束后,读取量筒所呈现的数据时,需要注意的三个主要问题是:一是要______,二是要调整量筒液面与广口瓶液面相平,三是要使视线与量筒内的凹液面相平.
(5)若标准状况下,由实验步骤①得到的气体体积为10.08L,则合金中镁的质量分数为______.
(6)在“amol/L稀硫酸”中a的值为______.
(7)请在图中画出实验步骤②中生成沉淀的物质的量(n)随加入氢氧化钠溶液的体积[v(NaOH)]的变化曲线.
参考答案:(1)实验装置中用于硫酸和合金反应的容器是原地烧瓶,故答案为
本题解析:
本题难度:一般
2、选择题 下列有关物质分离、提纯方案正确的是( )
A.除去铁粉中混有的I2:加热使I2升华
B.除去NaCl固体中混有的MgCl2:加入KOH溶液后过滤,滤液蒸发结晶
C.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤
D.除去AgI中的AgCl:将混合物置于浓KI溶液中一段时间后过滤并洗涤沉淀
参考答案:A.Fe与I2在加热条件下反应生成FeI2,不符合除杂的原则
本题解析:
本题难度:一般
3、实验题 将试管放人盛有25℃饱和石灰水的烧杯中,试管中开始放入小块镁片,再用滴管滴人5 mL盐酸于试管中,试回答下列问题:
(1)实验中观察到的现象是_____________________。
(2)产生上述现象的原因是_____________________。
(3)写出有关反应的离子方程式__________________________。
(4)由实验推知,MgCl2溶液和H2总能量_____________(填“大于”、“小于”或“等于”)镁片和盐酸的总能量。
参考答案:(1)试管中镁片逐渐溶解,有大量气泡产生,烧杯中有固体析出<
本题解析:
本题难度:一般
4、实验题 如图是某同学设计的放热反应的观察装置。?

其实验顺序是:
①按图所示将实验装置连接好。
②在U形管内加入少量红墨水(或品红)溶液。打开T型管螺旋夹,使U形管内两边的液面处于同一水平面,再夹紧螺旋夹。
③在中间的试管里盛1 g氧化钙,当滴入2 mL左右的蒸馏水后,同时打开螺旋 夹即可观察。
试回答:
(1)实验中观察到的现象是_________ 。
(2)该实验中在安装好装置后必须进行的第一步实验操作是___________ 。
(3)实验中反应的化学反应方程式是____________ 。
(4)说明CaO、H2O的能量之和_________Ca(OH)2的能量。(填“>”、“<”或“=”)
(5)若该实验中CaO换成NaCl,实验还能否观察到相同现象?_________________ 。
参考答案:(1)U形玻璃管里的红墨水(或品红)会沿开口端上升
本题解析:
本题难度:一般
5、实验题 (12分)某研究性小组用0.20 mol/L NaOH溶液滴定未知浓度的白醋(指示剂为酚酞)。
请回答:
(1)下图表示50 ml滴定管中液面的位置,若A与C刻度间相差1ml,A处的刻度为20,此时滴定管中液体的体积????????????????????????????mL。
(2)滴定过程中,眼睛始终注视 ?????????????????????????????,直到锥形瓶中液体的颜色……。
 ?????
?????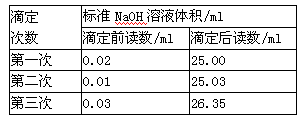
(3)同学们进行了三次实验,每次取白醋 20.00 ml, 实验结果记录如上表:请计算白醋的物质的量浓度为_________????????(保留两位有效数字)。
(4)操作时用白醋润洗锥形瓶,对滴定结果产生的影响是________(填“偏大”或“偏小”或“无影响”。下同)。若用白醋润洗酸式滴定管,对滴定结果产生的影响是???????。
(5)若滴定终点时测得pH=7。下列离子浓度的比较正确的是??????????。
A.c(Na+)>c(CH3COO―)
B.c(Na+)<c(CH3COO―)
C.c(Na+)=c(CH3COO―)
D.不能确定
参考答案:(12分)(1)>29.60Ml??(2)锥形瓶中液体颜色的
本题解析:
试题分析:(1)滴定管的刻度自上而下是逐渐增大的,且能准确读数到0.1ml,所以根据图中刻度线的位置可知,此时滴定管中液体的体积大于50.00ml-20.40ml=29.60ml。
(2)滴定过程中,眼睛始终注视锥形瓶中液体颜色的变化,直到锥形瓶中液体的颜色发生变化。
(3)根据表中数据可知,三次实验中消耗氢氧化钠溶液的体积分别是24.98ml、25.02mol、26.32ml,显然第三次的实验误差太大,舍去,则实际消耗氢氧化钠溶液体积的平均值是(24.98ml+25.02mol)÷2=25.00ml,所以白醋的物质的量浓度是 。
。
(4)操作时用白醋润洗锥形瓶,则消耗氢氧化钠溶液的体积增加,则滴定结果偏大。若用白醋润洗酸式滴定管,则测定结果不影响。
(5)根据电荷守恒可知c(Na+)+c(H+)=c(OH―)+c(CH3COO―),由于溶液显中性,则c(H+)=c(OH―),所以c(Na+)=c(CH3COO―),答案选C。
点评:该题是中等难度的试题,试题基础性强,难易适中,贴近高考。该题在注重对学生基础性知识巩固与训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和灵活应变能力。该题的难点在于误差分析和离子浓度大小比较。
本题难度:一般