微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 把4mol A和2.5mol B混合于2L密闭容器中,发生反应:3A(g)+2B(s)  xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol?L-1?min-1 ,下列结论错误的是(????? )
xC(g)+D(g),5min后反应达到平衡,容器内压强变小,测得D的平均反应速率为0.05mol?L-1?min-1 ,下列结论错误的是(????? )
A.A的平均反应速率为0.15 mol?L-1?min-1
B.平衡时,C的浓度为0.25mol?L-1
C.B的平均反应速率为0.1 mol?L-1?min-1
D.平衡时,容器内压强为原来的0.875倍
2、简答题 在一体积为1L的容器中,通入一定量的N2O4,在100℃时发生如下反应,N2O4?

2NO2-Q(Q>0),其N2O4?和NO2?浓度变化如图如示.
(1)上述反应的平衡常数表达式为______,升高温度K值______(填“增大”、“减小”或“不变”)]
(2)在0-60s这段时间内,四氧化二氮的平均反应速率为______mol/L.s
(3)120℃时,在相同的容器中发生上述反应,容器内各物质的物质的量变化如图
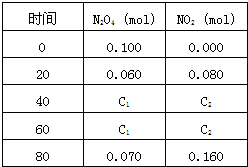
①该温度时,反应处于平衡状态的时间是______,C1的数值______0.04(填“大于”、“小于”或“等于”).
②反应在60-80s间平衡向逆反应方向移动,可能的原因是______
(A)?使用催化剂????(B)?减少N2O4的浓度
(3)减小体系压强???(D)?增加NO2的浓度.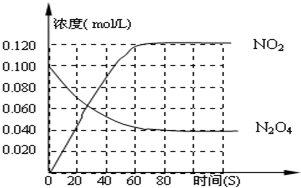
3、选择题 下列叙述中,正确的是( )
A.在船舶的外壳装上铜块可防止其发生电化学腐蚀
B.MnO2、FeCl3和CuSO4都可加快H2O2的分解速率
C.FeCl3溶液和Fe2(SO4)3溶液加热蒸干、灼烧都得到Fe2O3
D.用惰性电极分别电解CuCl2溶液和MgCl2溶液分别得到单质Cu和Mg
4、填空题 某学生为了探究锌与盐酸反应过程中速率变化。在100mL稀盐酸中加入足量的锌粉,标准状况下测得数据累计值如下: