微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 常温下,将10.0 g 40%的NaCl溶液跟40.0 g 15%的NaCl溶液混合,得到密度为1.17 g・cm-3的混合液,该混合液NaCl的质量分数为?????????????,物质的量浓度为???????????????。
参考答案:20%??????????? 4 mol・L-1(不带单位不
本题解析:略
本题难度:简单
2、简答题 实验室要配制0.1mol/L的Na2CO3(aq)500mL.
(1)需要称取Na2CO3粉末的质量为______.
(2)配制上述溶液除需要托盘天平(带砝码)、药匙、玻璃棒、烧杯外,还需要的仪器有______、______.
(3)配制过程中,若未洗涤烧杯和玻璃棒,则所配制溶液的浓度将______(填“偏高”、“偏低”或“不影响”).
参考答案:(1)500mL 0.1mol/L的Na2CO3溶液中含有碳
本题解析:
本题难度:简单
3、选择题 设nA为阿伏加德罗常数的数值,下列说法正确的是
A.通常状况下,22.4 L CCl4含有4nA个Cl原子
B.常温常压下,18 g H2O中含有2nA个氢原子
C.0.1 mol・L-1NaCl溶液中含有0.1nA个Na+
D.7.8 g Na2O2与足量水反应转移0.2nA个电子
参考答案:B
本题解析:
试题分析:通常状况下,22.4 L CCl4的物质的量不是1mol,故A正确;18 g H2O的物质的量是1mol,含有2nA个氢原子,故B正确;没有溶液的体积,所以不能求溶质的物质的量,故C错误;7.8 g Na2O2与足量水反应转移0.1nA个电子,故D错误。
考点:本题考查阿伏伽德罗常数。
本题难度:一般
4、填空题 (13分)下图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容。

据此回答下列问题:
(1)该硫酸的物质的量浓度为 mol/L。
(2)配制250mL 0.92mol・L-1的稀硫酸需取该硫酸 mL。
(3)配制时必需的玻璃仪器有:
(4)定容时,若加入的水超过刻度线,必须采取的措施是
(5)下列操作对H2SO4的物质的量浓度有什么影响(偏高、偏低或无影响)?
①转移溶液后,未洗涤烧杯: ;(1分)
②容量瓶用水洗净后未烘干: ; (1分)
③定容时俯视容量瓶的刻度线: 。(1分)
(6)在配置过程中,下列操作不正确的是(填序号) 。
A.使用容量瓶前检查它是否漏水
B.容量瓶用蒸馏水洗净后,再用待配液润洗
C.将氢氧化钠固体放在天平托盘的滤纸上,准确称量并放入烧杯中溶解.
D.将准确量取的18.4mol・L-1的硫酸,注入已盛有30mL水的100mL的容量瓶中,加水至刻度线
E.定容后塞好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转摇匀
参考答案:(1)18.4
本题解析:
试题分析: 本题属于浓溶液的稀释,需先根据公式c=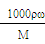 确定浓度为18.4mol/L;溶液稀释过程中溶质的物质的量不变,求得需要浓硫酸的体积为12.5mL,(5)属误差分析,需根据c=
确定浓度为18.4mol/L;溶液稀释过程中溶质的物质的量不变,求得需要浓硫酸的体积为12.5mL,(5)属误差分析,需根据c=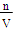 进行,未洗涤烧杯,导致n偏小,结果偏低;定容时俯视刻度线导致V偏小,结果偏高。(6)中容量瓶不需润洗;因为氢氧化钠易潮解,称量时需放入烧杯中;容量瓶不能用来溶解物质或稀释溶液。
进行,未洗涤烧杯,导致n偏小,结果偏低;定容时俯视刻度线导致V偏小,结果偏高。(6)中容量瓶不需润洗;因为氢氧化钠易潮解,称量时需放入烧杯中;容量瓶不能用来溶解物质或稀释溶液。
考点: 物质的量浓度溶液的配制、误差分析。
本题难度:一般
5、选择题 下列有关摩尔的使用正确的是( )
A.1mol O的质量为16g・mol-1
B.0.5mol He约含有6.02×1023个电子
C.2H既表示2个氢原子又表示2mol氢原子
D.每摩尔物质均含有6.02×1023个原子
参考答案:B
本题解析:
试题分析:A.1mol O的质量为16g,错误;B.He是2号元素,He是单原子分子,所以0.5mol He约含有6.02×1023个电子,正确;C.2H表示2个氢原子,错误;D.每摩尔物质均含有6.02×1023个组成该物质的基本微粒,错误。
考点:考查有关摩尔的使用的正误判断的知识。
本题难度:一般