微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 关于化学反应与能量的说法正确的是(??)
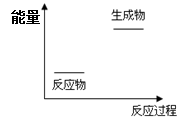
A.根据右图提供的信息,该反应是放热反应
B.化学变化中的能量变化主要由化学键变化引起的
C.化学反应中只伴随热量的变化
D.CaCO3(s)==CaO(s)+CO2(g) ΔH="+178.5" KJ・mol-1的意义是表示1mol CaCO3完全分解生成1mol CaO和1mol CO2气体要放出178.5 KJ的热量
参考答案:B
本题解析:
试题分析:A、根据图示信息可以看出生成物的能量高于反应物的能量,反应是吸热反应,故A错误;
B、化学反应中旧键的断裂吸收能量,新键的生成释放能量,并且二者不相等,所以化学变化中的能量变化主要由化学键变化引起的,故B正确;
C、化学反应伴随物质变化的同时一定伴随能量变化,故C错误;
D、△H>0表示反应为吸热反应,故D错误.
故选B。
点评:本题考查学生有关化学反应中的能量变化知识,可以根据所学知识来进行,难度不大。
本题难度:一般
2、填空题 在下列物质中:①NaOH、②H2O2、③NH4Cl、④Na2O2、⑤C2H2、⑥SiC晶体?⑦Na2S⑧单晶硅。用序号回答下列问题:
⑴含有极性共价键的原子晶体是?????;
⑵只含有离子键的离子晶体是?????;
⑶既含有离子键又含有非极性共价键的离子晶体是?????;
⑷ 既含有离子键,又含有极性共价键和配位键的离子晶体是?????;
⑸含有极性共价键和非极性共价键的非极性分子是?????;
⑹含有极性共价键和非极性共价键的极性分子是?????。
参考答案:(各2分共12分)⑴ ⑥ , ⑵ ⑦ ,⑶ ④, ⑷ ③ ,
本题解析:
试题分析:一般活泼的金属和活泼的非金属容易形成离子键,非金属元素的原子间容易形成共价键。离子间通过离子键形成的晶体是离子晶体,分子间通过分子间作用力形成的晶体是分子晶体,原子间通过共价键形成的空间网状结构的晶体是原子晶体,由金属阳离子和自由电子构成的晶体是金属晶体,据此可知:
⑴含有极性共价键的原子晶体是碳化硅,答案选⑥;
⑵只含有离子键的离子晶体是硫化钠,答案选⑦;
⑶既含有离子键又含有非极性共价键的离子晶体是过氧化钠,答案选④;
⑷ 既含有离子键,又含有极性共价键和配位
本题难度:一般
3、填空题 (2014届甘肃省玉门市油田一中高三第三次摸底考试化学试卷)
碳和碳的化合物在生产、生活中的应用非常广泛,在提倡健康生活已成潮流的今天,“低碳生活”不再只是一种理想,更是一种值得期待的新的生活方式。
(1)甲烷燃烧放出大量的热,可作为能源用于人类的生产和生活。
已知:①2CH4(g)+3O2(g)=2CO(g)+4H2O(l) △H=" ―1214" kJ/mol
②2CO(g)+O2(g)=2CO2(g) △H=" ―566" kJ/mol
则表示甲烷燃烧热的热化学方程式 。
(2) 将两个石墨电极插入KOH溶液中,向两极分别通入CH4和O2,构成甲烷燃料电池。其负极电极反应式是: 。
(3)某同学利用甲烷燃料电池设计了一种电解法制取Fe(OH)2的实验装置(如下图所示),通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法中正确的是 (填序号)
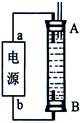
A.电源中的a一定为正极,b一定为负极
B.可以用NaCl溶液作为电解液
C.A、B两端都必须用铁作电极
D.阴极发生的反应是:2H+ + 2e-= H2↑
(4)将不同量的CO(g)和H2O(g)分别通入体积
为2L的恒容密闭容器中,进行反应:
CO(g)+H2O(g)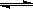 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组
| 温度/℃
| 起始量/mol
| 平衡量/mol
| 达到平衡所需时间/min
|
H2O
| CO
| CO2
|
1
| 650
| 2
| 4
| 1.6
| 5
|
2
| 900
| 1
| 2
| 0.4
| 3
|
3
| 900
| 1
| 2
| 0.4
| 1
①实验1中,以v (H2)表示的平均反应速率为 。
②实验3跟实验2相比,改变的条件可能是 (答一种情况即可)
参考答案:(1)CH4(g)+2O2(g) 本题解析: 本题解析:
(1)甲烷完全燃烧生成二氧化碳气体和液态水,所以甲烷燃烧热的热化学方程式中甲烷的物质的量是1mol,将①②相加除以2可得,答案是CH4(g)+2O2(g) CO2(g)+2H2O(l) △H1=―890KJ.mol-1 CO2(g)+2H2O(l) △H1=―890KJ.mol-1
(2)负极发生氧化反应,所以甲烷在负极发生氧化反应,结合电解质溶液,负极的电极反应式为CH4- 8e-+ 10 OH- CO32-+ 7H2O; CO32-+ 7H2O;
(3)A、电解过程中两极分别是H+和Fe放电生成氢气和亚铁离子,所以两极哪端都可以生成氢气,a不一定为正极,b不一定为负极,但a为正极,b为负极,效果较好,错误;B、在装置中铁一定作阳极,所以氯化钠溶液是电解质溶液,不影响阳极Fe放电生成亚铁离子,阴极H+放电生成氢气,正确;C、装置中铁一定作阳极,阴极可以是铁,也可以是其他惰性电极,错误;D、阴极H+放电生成氢气,正确,答案选BD。
(4)①实验1中,CO2的浓度增加0.8mol/L,所以氢气浓度也增加0.8mol/L,v (H2)= 0.8mol/L/5min=0.16mol/(L・min);
②实验3跟实验2相比,到达平衡时间缩短,说明反应速率加快,反应温度、各物质的物质的量均未变,所以可能是使用了催化剂或增大压强。
本题难度:一般
4、选择题 关于化学键的下列叙述中正确的是( )
A.化学键存在于相邻原子之间,是一种强相互引力作用
B.化学键可存在于不同种元素的原子之间,也可存在于同种元素的原子之间
C.化学键中原子间强烈作用的实质是万有引力作用
D.单质中一定存在化学键作用
参考答案:A、化学键通常指的是相邻的两个或多个原子之间的强烈的相互作用
本题解析:
本题难度:简单
5、选择题 已知在101KPa,298K条件下,2 mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是(??)
A.H2O(g)= H2(g)+ 1/2O2;△H(298K) = -242kJ・mol-1
B.H2(g)+ 1/2O2(g)= H2O(l);△H(298K) = +484kJ・mol-1
C.H2(g)+ 1/2O2(g)= H2O(g);△H(298K) = -242kJ・mol-1
D.H2(g)+ 1/2O2(g)= H2O(g);△H(298K) = -484kJ
参考答案:C
本题解析:该题考查热化学方程式书写的注意事项。最常见的错误有:①未注明物质的聚集状态,②系数与△H的值不相同,③△H的符号相反了。在298K时,1mol的H2(g)和0.5mol O2(g)反应生成1mol的H2O(l)放出285.8kJ的热量。由“2 mol氢气燃烧生成水蒸气放出484KJ热量”知“1 mol氢气燃烧生成水蒸气放出242kJ热量”。
本题难度:简单
|