微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 接触法制硫酸的生产过程中,下列措施能提高硫酸的产率的是()
A.控制接触室内的温度在450℃左右
B.沸腾炉中通入过量空气
C.对炉气进行除尘、洗涤、干燥处理
D.接触室中用V2O5作催化剂
参考答案:B
本题解析:通入过量空气,可以使矿石燃烧充分而提高硫酸的产率,B符合题意;对炉气进行除尘、洗涤、干燥处理的目的是防止催化剂中毒,不能提高硫酸的产率,C不符合题意;接触室中用V2O5作催化剂和控制接触室内的温度在450 ℃左右,都只能提高化学反应的速率,不能提高硫酸的产率,A、D不符合题意。
本题难度:简单
2、选择题 下列离子方程式中,正确的是(???)
A.金属钠与冷水反应:Na+2H2O====Na++2OH-+H2↑
B.碳酸钙投入醋酸溶液中CaCO3+2CH3COOH====Ca2++2CH3COO-+H2O+CO2↑
C.向Ca(ClO)2溶液中通过量CO2气体:Ca2++2ClO-+CO2+H2O====CaCO3↓+2HClO
D.向硫酸铜溶液中滴入Ba(OH)2溶液:Ba2++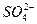 ====BaSO4↓
====BaSO4↓
参考答案:B
本题解析:A项中离子方程式没有配平;C项中应该生成Ca(HCO3)2,而不是CaCO3;D项中离子方程式应该是:Cu2++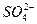 +Ba2++2OH-====Cu(OH)2↓+BaSO4↓。所以B正确。
+Ba2++2OH-====Cu(OH)2↓+BaSO4↓。所以B正确。
本题难度:简单
3、选择题 下列说法中正确的是?( )
A.6.8 g固体KHSO4与3.9 g固体Na2O2中阴离子数目相同
B.常温下铁、铜均不溶于浓硫酸, 说明常温下铁、铜与浓硫酸均不反应
C.离子化合物中只含离子键
D.中子数为18的氯原子可表示为18Cl
参考答案:A
本题解析:
试题分析:KHSO4=K++HSO4-。n(KHSO4)="0.05" mol.所以n(HSO4-)="0.05" mol; Na2O2=2Na++O22-.n(Na2O2)=" 0.05" mol,所以所以n(O22-)="0.05" mol;因此阴离子数目相同。正确。B.常温下铁不溶于浓硫酸,是因为Fe在常温下在浓硫酸中会被氧化产生一层致密的氧化物保护膜,阻止了反应的继续减小,而铜不溶于浓硫酸是因为没有达到铜与浓硫酸反应所需要的温度。原因不同。错误。C.离子化合物中一定含离子键,可能含有共价键
本题难度:一般
4、选择题 下列关于硫的说法不正确的是(???)
A.硫有多种同素异形体
B.硫的化学性质与氧气相同
C.S与Fe反应生成FeS
D.S与Cu反应生成Cu2S
参考答案:B
本题解析:硫有S4、S6、S8等多种同素异形体,硫的化学性质与氧气相似;O2的氧化性大于S,O2与Cu反应生成CuO,而S与Cu反应生成Cu2S,故B项错误。
本题难度:简单
5、实验题 常温下,将Fe粉和S粉混合,不发生反应.某课外活动小组将Fe粉和S粉按物质的量比1∶1混合均匀,并置于水平放置且隔绝空气的玻璃管中,加热片刻,反应开始,然后撤去酒精灯,发现反应仍能剧烈进行,并使生成的固体呈红热状态.试回答:
(1)上述现象说明了_______________________.
(2)将生成的黑色固体置于稀H2SO4中,有气体放出,写出发生反应的离子方程式______.
(3)已知H2S是一种剧毒、有刺激性气味的气体,试说明实验室制取H2S时应采用的一条安全措施:___________________.
参考答案:(1)Fe与S的反应是放热反应 (2)FeS+2H+=Fe2
本题解析:(1)撤去酒精灯,反应仍能继续,表明有热量来源.热量何来?只能说反应是放热反应。
(2)FeS与H2SO4发生复分解反应。(3)应将多余的H2S吸收或通过通风橱排走,以免中毒。
本题难度:简单