微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 实验室里需要配制480mL 0.10mol・L-1的硫酸铜溶液,下列实验方案及实验操作正确的是(???)
?
| 容量瓶容积
| 溶质质量
| 实验操作
|
A
| 480mL
| 硫酸铜:7.68g
| 加入 500mL水
|
B
| 480mL
| 胆矾:12.0g
| 配成500mL溶液
|
C
| 500mL
| 硫酸铜:8.0g
| 加入500mL水
|
D
| 500mL
| 胆矾:12.5g
| 配成500mL溶液
?
参考答案:D
本题解析:略
本题难度:简单
2、实验题 某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质。某化学课外小组设计以下流程,以该矿样为原料生产CuCl2?2H2O晶体。
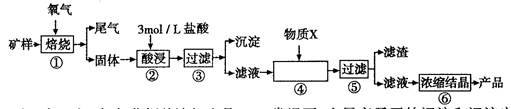
已知:在20℃时,氯化铜的溶解度是73g;常温下,金属离子开始沉淀和沉淀完全时的pH见下表。
金属离子
| 开始形成氢氧化物沉淀的pH
| 完全形成氢氧化物沉淀的pH
| Fe2+
| 7.0
| 9.0
| Fe3+
| 1.9
| 3.2
| Cu2+
| 4.7
| 6.7
回答下列问题:
(1)步骤①的焙烧过程中需要通入氧气。在实验室中使用中学化学常见物质、下图所示装置制取氧气,试写出你熟悉的、符合上述条件的两个化学方程式

(2)在焙烧过程中还有废气产生,其中一种是主要的大气污染物。
若在实验室中以碱液吸收处理之,下列A、B、C装置中可行的是____(填字母);若选用甲装置,则烧杯中的下层液体可以是??????????
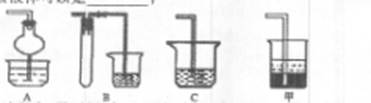
(3)步骤②酸浸过程中,需要用到3 mollL的盐酸l00mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有____;
(4)步骤④加入物质X的目的是???????,物质X可以选用下列物质中的???????;
A.氧化铜??? B.稀盐酸??? C.氨水?? D.氧化亚铁
(5)在整个生产流程中,共需要进行??????????????次过滤操作。
参考答案:(1)2H2O2 = 2H2O+O2↑,2Na2O2 + 2
本题解析:(1)根据装置图可知是固液不加热制气体,所以用H2O2和Na2O2来制取O2反应方程式为:2H2O2 = 2H2O + O2 ↑,2Na2O2 + 2H2O ="4NaOH" + O2 ↑
(2)尾气中含有的是SO2,SO2为酸性氧化物,极易溶于水,可由碱液吸收,但易形成倒吸,故可采用AB装置防倒吸:A中的干燥管可缓冲倒吸、B装置中的试管可做安全瓶;
若选用甲装置,可采用密度大于水的有机溶剂,例如四氯化碳,也可起到防倒吸的作用
(3)配制盐酸一般采取稀释的方法,用量筒量取一定的浓盐酸;
还需要选用100 mL容量瓶的容量瓶进行配制
(4)根据氢氧化物开始沉淀和完全沉淀的pH可知,只要调节pH值,就可以Fe3+以Fe(OH)3沉淀的形式析出,达到除杂的目的。为了不引入新杂质,还能调节pH值,所以选铜的难溶物,如CuO、Cu(OH)2、CuCO3等
(5)除了图示的两次过滤操作外,对CuCl2浓缩结晶后,还需要过滤才可得到产品,故共需要三次过滤操作
本题难度:一般
3、实验题 工业上将纯净干燥的氯气通入到物质的量浓度为0.375mol/LNaOH溶液中得到漂水。某同学想在实验室探究Cl2性质
并模拟制备漂水,下图是部分实验装置。已知KMnO4与盐酸溶液反应可以制取Cl2。

(1)配制物质的量浓度为0.375 mol/LNaOH溶液时,主要用到的玻璃仪器有烧杯、玻璃棒、胶头滴管、量筒和 。
(2)浓硫酸的作用是 。
(3)装置E中发生化学反应的离子方程式为 。
(4)装置B中饱和NaCl溶液可用于除去Cl2中的HCl气体,已知氯气与水的反应是一个可逆反应,请简述饱和NaCl溶液除去Cl2
中HCl气体的原理(用离子方程式表示和文字说明) 。
(5)实验时装置D中湿润的红色纸条褪色,干燥部分没有褪色,放置一段时间后,纸条全部褪色。该同学认为Cl2的密度比空气大,
可能是试管下部Cl2的浓度大于试管上部Cl2的浓度所导致的。请判断该解释是否合理,并分析产生上述实验现象的原因 ;
如需改进,请简述设计方案 (若认为合理。则此问可不答)。
参考答案:(12分)(1)容量瓶?????????(2)干燥氯气
本题解析:实验目的是制氯气并检验氯气的性质。Cl2(HCl/H2O)饱和氯化钠溶液吸收氯气中的氯化氢气体,浓硫酸干燥氯气。使纸条褪色的是次氯酸,不是氯气。
本题难度:一般
4、实验题 氢溴酸在医药和石化工业上有广泛用途。下图是模拟工业制备氢溴酸粗品并精制的流程
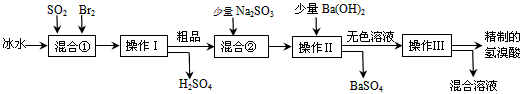
根据上述流程回答下列问题:
(1)混合①中发生反应的化学方程式为_________________________。
(2)混合①中使用冰水的目的是_________________________。
(3)操作Ⅱ和操作Ⅲ的名称分别是____________________、_________________。
(4)混合②中加入Na2SO3的目的是_________________________。
(5)纯净的氢溴酸应为无色液体,但实际工业生产中制得的氢溴酸(工业氢溴酸)带有淡淡的黄色。于是甲乙两同学设计了简单实验加以探究:
甲同学假设工业氢溴酸呈淡黄色是因为含Fe3+,则用于证明该假设所用的试剂为_________________,若假设成立可观察到的现象为_________________________。乙同学假设工业氢溴酸呈淡黄色是因为
________________,其用于证明该假设所用的试剂为_____________。
参考答案:(1)SO2+Br2+2H2O==2HBr+H2SO4
本题解析:
本题难度:困难
5、实验题 菠菜是一种高效的补铁剂。长期以来民间流传有“菠菜不能与豆腐同食”“菠菜根比菠菜茎叶更有营养”等说法。 某学校化学兴趣小组的同学拟通过实验探究以下问题:
①菠菜是否含有丰富的铁?
②菠菜是否含有草酸类物质?
③菠菜根中铁的含量是否比菠菜茎和叶的高?
该同学通过上网查询,获得以下资料:草酸又名乙二酸,其酸性比乙酸稍强,草酸及其盐具有较强的还原性,其中草酸钙不溶于水。 他们设计的实验步骤如下
Ⅰ.
Ⅱ.取菠菜根ag使用相同仪器、试剂,重复I中实验,观察实验现象。
Ⅲ.将菠菜在少量开水中煮沸2~3 min,冷却后滤去菠菜,得滤液。向滤液中加入足量Ca(OH)2溶液,然后再加入足量试剂X,观察现象。请回答以下问题:
(1)操作①中使用的仪器除三脚架、酒精灯、玻璃棒、坩埚钳、泥三角外还需要________,操作②的名称是________;
(2)可以说明菠菜中含Fe元素的现象是____;可以说明菠菜根中Fe元素含量要比菠菜茎叶中多的现象是
____________________。
(3)菠菜中的Fe元素是+2价还是+3价?____________________
(4)通过步骤Ⅲ可以确定菠菜中含有草酸类物质。由于滤液中含有CO32-,故需加入试剂x排除CO32-的干扰。则x是________________(写化学式),加入试剂X后观察到的现象是________________。
(5)你认为“菠菜不能与豆腐同食”的原因是________________。
参考答案:(1)坩埚;过滤
(2)步骤I中得到溶液加KSCN后
本题解析:
本题难度:一般
|
|