微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 300°C时,将2 mol A和2 mol B两种气体混合于2 L密闭容器中,发生如下反应:3A(g)+B(g) 2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
2C(g)+2D(g) ΔH=Q,2 min末达到平衡,生成0.8 mol D。
(1)300°C时,该反应的平衡常数表达式为K=________。已知K300°C<K350°C,则ΔH________0(填“>”或“<”)。
(2)在2 min末时,B的平衡浓度为_______,D的平均反应速率为_______。
(3)若温度不变,缩小容器容积,则A的转化率________(填“增大”“减小”或“不变”),原因是__________________________________________。
(4)如果在相同的条件下,上述反应从逆反应方向进行,开始时若加入C、D各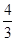 mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B________mol。
mol。若使平衡时各物质的物质的量浓度与原平衡相同,则还应该加入B________mol。
参考答案:(1)  本题解析:(1)若温度越高,K越大,则说明升温,平衡正向移动,即正反应为吸热反应,ΔH>0。(2)生成0.8 mol D,则反应掉0.4 mol B,剩余1.6 mol B,c(B)=1.6 mol÷2 L=0.8 mol・L-1。v(B)=
本题解析:(1)若温度越高,K越大,则说明升温,平衡正向移动,即正反应为吸热反应,ΔH>0。(2)生成0.8 mol D,则反应掉0.4 mol B,剩余1.6 mol B,c(B)=1.6 mol÷2 L=0.8 mol・L-1。v(B)= =0.1 mol・L-1・min-1,由化学计量数知,D的反应速率应为B的2倍,故v(D)=2v(B)=2×0.1 mol・L-1・min-1=0.2 mol・L-1・min-1。(3)该反应为反应前后气体的总物质的量不变的反应,加压平衡不移动,故A的转化率不变。(4)将C、D折算成A、B,则相当于加入2 mol A和2/3 mol B,容器体积固定,若浓度相同,则说明起始时物质的量相等,故B还应加入2 mol-
=0.1 mol・L-1・min-1,由化学计量数知,D的反应速率应为B的2倍,故v(D)=2v(B)=2×0.1 mol・L-1・min-1=0.2 mol・L-1・min-1。(3)该反应为反应前后气体的总物质的量不变的反应,加压平衡不移动,故A的转化率不变。(4)将C、D折算成A、B,则相当于加入2 mol A和2/3 mol B,容器体积固定,若浓度相同,则说明起始时物质的量相等,故B还应加入2 mol-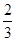 ?mol=
?mol=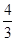 ?mol。
?mol。
本题难度:一般
2、简答题 在一定温度下,将2molA和2molB两种气体相混合于容积为2L的某密闭容器中,发生如下反应:
3A(g)+B(g)?xC(g)+2D(g),2min末反应达到平衡状态,生成了0.8molD,并测得C的浓度为0.4mol/L,请填写下列空白:
(1)x值等于______
(2)A的转化率为______
(3)如果增大反应体系的压强,则平衡体系中C的质量分数______(填增大、减小或不变)
(4)在此温度下,该化学反应的平衡常数的值为:k=______
(5)如果上述反应在相同条件下从逆反应开始进行,开始加入C和D各
4
3
mol,要使平衡时各物质的质量分数与原平衡时完全相等,则还应加入______物质______mol.
参考答案:(1)平衡时C的浓度为0.4mol/L,故生成C的物质的量为
本题解析:
本题难度:一般
3、选择题 可逆反应:4A(s)+3B(g)?2C(g)+D(g)(放热反应),2s末,B的浓度减小0.6mol/L,下列说法正确的是( )
A.在2s时,A与B物质反应速率之比为4:3
B.其他条件不变,升高温度,正反应速率减小,逆反应速率增大
C.在2s时,D的物质的量一定增加0.2mol
D.若容器的温度和体积保持不变,反应前后容器的压强相等
参考答案:A、由于A物质为固体,不能用来表示反应速率,故A错误;
本题解析:
本题难度:简单
4、选择题 T℃时,某一气态平衡体系中含有X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为: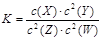 ,有关该平衡体系的说法正确的是 ,有关该平衡体系的说法正确的是
A.该反应可表示为X(g) + 2Y(g) 2Z(g) + 2W(g) 2Z(g) + 2W(g)
B.减小X浓度,平衡向逆反应方向移动,平衡常数K减小
C.增大反应容器的压强,该反应速率一定增大
D.升高温度,W(g)体积分数增加,则正反应是放热反应
参考答案:D
本题解析:
试题分析:A.由于化学平衡常数是可逆反应达到平衡状态时各生成物浓度幂指数的乘积与各反应物浓度幂指数乘积的比。所以该反应可表示为2Z(g) + 2W(g)  X(g) + 2Y(g)。错误。B. 减小X浓度,平衡向正反应方向移动,但是由于反应的温度不变,所以化学平衡常数K不变。错误。C.若容器的容积不变,向容器内冲入与体系无关的气体而增大反应容器的压强,由于各物质的浓度没变,所以该反应速率不变;若缩小容器的容积,使物质的浓度增大,则化学反应速率加快。错误。D.根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。由于W(g)体积分数增加,则升高温度平衡逆向移动逆反应为吸热反应。则正反应是放热反应。正确。 X(g) + 2Y(g)。错误。B. 减小X浓度,平衡向正反应方向移动,但是由于反应的温度不变,所以化学平衡常数K不变。错误。C.若容器的容积不变,向容器内冲入与体系无关的气体而增大反应容器的压强,由于各物质的浓度没变,所以该反应速率不变;若缩小容器的容积,使物质的浓度增大,则化学反应速率加快。错误。D.根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。由于W(g)体积分数增加,则升高温度平衡逆向移动逆反应为吸热反应。则正反应是放热反应。正确。
本题难度:一般
5、选择题 可逆反应2SO2+O2 2SO3达到平衡的标志是( )。 2SO3达到平衡的标志是( )。
①消耗2 mol SO2的同时生成2 mol SO3 ②SO2、O2与SO3的物质的量之比为2∶1∶2 ③反应混合物中,SO3的质量分数不再改变
A.①②
B.①③
C.③
D.①
参考答案:C
本题解析:①只提到正反应速率;②各物质的物质的量之比为2∶1∶2,若为瞬时,不一定平衡,如保持不变,则平衡;③SO3的质量分数不再改变,即说明各物质浓度不再改变,反应达到平衡。
本题难度:简单
|