微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 同质量的下列气体中,所含原子数最多的是
A.CH4
B.CO2
C.H2S
D.N2
参考答案:A
本题解析:
试题分析:根据公式:N=n/NA=m/(MNA),题中已知质量(m)相等,NA又相等,带入公式计算,A项:原子数为5m/(16NA);B项:原子数为3m/(44NA);C项:原子数为3m/(34NA);D 项:原子数为2m/(28NA)。故选A。
考点:化学计算
点评:本题考查的是物质的量在化学计算中的应用,学生要熟悉阿弗加德罗常数、质量、物质的量、粒子数之间的换算,问题就迎刃而解了。
本题难度:一般
2、填空题 (6分)等物质的量的CO和CO2所含分子数之比为_____________,所含氧原子数之比为______,
质量之比为_____________。
参考答案:1:1 , 1:
本题解析:
试题分析:物质的量之比等于分子数之比,相同物质的量的CO和CO2,分子数之比为1:1;相同物质的量的CO和CO2,假设都为1mol,则所含氧原子数之比为1∶2,质量分别为28g和44g,所以质量比为7:11。
考点:本题考查物质的量。
本题难度:一般
3、选择题 由乙烯和乙醇蒸气组成的混和气体中,若碳元素的质量百分含量为60%,则氧元素的质量百分含量为( )
A.15.6%
B.26.7%
C.30%
D.无法确定
参考答案:乙烯的分子式为C2H4,乙醇的分子式为C2H6O,可将乙醇的
本题解析:
本题难度:简单
4、选择题 设NA为阿伏加德罗常数的值,下列叙述正确的是:( )
A.常温常压下,22.4 L乙烯中C―H键数为4 NA
B.1 mol羟基中电子数为10NA
C.在反应KIO3+6HI=KI+3I2+3H2O中,每生成3 mol I2转移的电子数为6 NA
D.常温下,1 L 0.1 mol/L NH4NO3溶液中NH4+的数目小于6.02×1022
参考答案:D
本题解析:
试题分析:A、常温常压下,22.4 L乙烯的物质的量不是1mol,分子中C―H键数不是4NA,A不正确;B、1mol羟基中电子数为9NA,B不正确;C、在反应KIO3+6HI=KI+3I2+3H2O中,碘酸钾中碘元素的化合价从+5价降低到0价,因此每生成3 mol I2转移的电子数为5NA,C不正确;D、硝酸铵溶于水铵根离子水解,因此常温下,1 L 0.1 mol/L NH4NO3溶液中NH4+的数目小于6.02×1022,D正确,答案选D。
本题难度:一般
5、简答题 实验室里要配制400mL0.2mol/L的硫酸钠溶液.实验步骤大致有:
A.在天平上称出______g硫酸钠固体,把它放在烧杯里,用适量的蒸馏水溶解.
B.把得到的溶液冷却后小心地沿着______注入______mL的容量瓶中.
C.用少量蒸馏水洗涤烧杯和玻璃棒2~3次,每次洗涤液也小心转入容量瓶中.
D.继续向容量瓶中加蒸馏水至液面距刻度l~2cm处,改用______小心滴加蒸馏水至溶液凹液面底部与刻度线水平相切.
E.将瓶塞塞紧,充分摇匀.
F.将配好的溶液倒入试剂瓶中,贴上标签,并洗涤容量瓶.
(1)请填写上述空白处.
(2)下列情况会使所配溶液浓度偏高的是______(填序号).
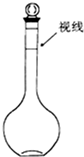
a.某同学定容时观察液面的情况如图所示
b.没有进行上述的操作步骤C
c.摇匀后发现液面低于刻度线又加水了
d.B操作时将少量液体洒到外面
e.容量瓶用前内壁沾有水珠
(3)如果实验室用18mol/L的浓硫酸配制3.6mol?L-1的稀硫酸250mL.计算所需浓硫酸的体积为______mL,在实验时应用______量取浓硫酸.
参考答案:(1)m=nM=CVM=0.2mol/L×0.5mol×14
本题解析:
本题难度:一般