微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 Na2FeO4是一种高效多功能水处理剂,一种制备Na2FeO4的方法可用化学方程式表示为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑,对此反应说法不正确的是
A.Na2O2在反应中既作氧化剂又作还原剂
B.O2是氧化产物
C.Na2FeO4既是氧化产物又是还原产物
D.2 mol FeSO4发生反应时,共有12 mol电子转移
参考答案:D
本题解析:
试题分析:6份的Na2O2中只有1份中的氧失去电子变成氧气,另外5份中的氧得到电子变成-2价的氧,A项错;2 mol Fe2+转化为+6价的铁时,转移8 mol电子,再加上生成1 mol O2时Na2O2失去的2 mol电子,反应中共转移10 mol电子,D错误。答案选D。
考点:氧化还原反应
本题难度:一般
2、选择题 下列有关说法正确的是
A.金属氧化物一定是碱性氧化物
B.BaSO4、CH3COOH、K2O、NH3?H2O都是电解质
C.工业上常用铝热反应来炼铁
D.二氧化硅不与任何酸反应,可用石英制造耐酸容器
参考答案:B
本题解析:分析:A、氧化铝属于金属氧化物,属于两性氧化物;
B、电解质是在水溶液和熔融状态下能导电的化合物;
C、工业上常用还原法来获得金属铁;
D、二氧化硅可以和唯一的酸HF酸反应.
解答:A、金属氧化物不一定是碱性氧化物,如氧化铝属于两性氧化物,七氧化二锰属于酸性氧化物,故A错误;
B、BaSO4、CH3COOH、NH3?H2O是在水溶液中能导电的化合物,K2O是在熔融状态能导电的化合物,均属于电解质,故B正确;
C、工业上常用焦炭或是一氧化碳还原氧化铁来获得金属铁,故C错误;
D、二氧化硅可以和唯一的酸HF酸反应,可以用石英制造耐酸容器,但是不能盛氢氟酸,故D错误.
故选B.
点评:本题涉及物质的分类、电解质的概念、金属的冶炼以及二氧化硅的性质知识,综合性较强,难度不大.
本题难度:困难
3、选择题 向三份均为100mL2mol/LNaHCO3溶液中,分别加入0.2g冰醋酸、0.1gCa(OH)2、0.3gNaAlO2固体(忽略溶液体积变化),则溶液中CO32-物质的量浓度的变化依次为
A.减小、减小、增大
B.减小、增大、增大
C.增大、减小、减小
D.减小、减小、减小
参考答案:A
本题解析:
本题难度:简单
4、填空题 (方程式每空2分,其余每空1分,共20分。)氧化还原反应和离子反应是高一所学过的重要化学反应类型,仔细思考回答下列问题:
(Ⅰ)下列一组有水参与的反应:
①2Na + 2H2O =" 2NaOH" + H2↑ ②2Na2O2 + 2H2O =" 4NaOH" + O2↑
③Na2O+ H2O =2NaOH ④3Fe+4H2O Fe3O4+4H2
Fe3O4+4H2
⑤2H2O 2H2↑+ O2↑ ⑥2F2 + 2H2O =" 4HF" + O2
2H2↑+ O2↑ ⑥2F2 + 2H2O =" 4HF" + O2
(1)其中不属于氧化还原反应的是 (填编号)
(2)在这些氧化还原反应中,水只作氧化剂的反应是 (填编号)
水只作还原剂的反应是 (填编号)
水既作氧化剂,又作还原剂是 (填编号)
水既不作氧化剂,又不作还原剂是 (填编号)
(3)根据你的理解,氧化还原反应的实质是( )
A.分子中的原子重新组合
B.氧元素的得失
C.电子的得失或共用电子对的偏移
D.化合价的改变
(4)请你运用所学知识分析3NO2+H2O = 2HNO3+NO是否属于氧化还原反应? (填“是”或“不是”),若是,这个反应的氧化剂和还原剂的质量比是 。
(Ⅱ)写出下列反应的离子方程式:
①铜片与稀硝酸的反应:
②过量二氧化碳通入澄清石灰水:
③往氯化铝溶液中加入过量的NaOH溶液:
(Ⅲ)写出下列反应的化学方程式:
①二氧化硫发生催化氧化反应:
②制漂白液的反应:
③雕刻花玻璃的反应:
参考答案:(Ⅰ)(1)③(1分) (2)①④;⑥;⑤;② (
本题解析:
试题分析:(Ⅰ)(1)①有元素化合价变化,属于氧化还原反应;②属于氧化还原反应;③没有化合价的变化,不属于氧化还原反应;④属于氧化还原反应;⑤属于氧化还原反应;⑥属于氧化还原反应。所以不属于氧化还原反应的有③。(2)①水做氧化剂;②水不是氧化剂也不是还原剂;④水是氧化剂;⑤水既是氧化剂又是还原剂;⑥水是还原剂。所以水只做氧化剂的选①④,水只做还原剂的选⑥,水既做氧化剂又做还原剂的选⑤,水不做氧化剂又不做还原剂的选②。(3)氧化还原反应的实质是电子得失或公用电子对的偏移,选C。(4)反应中氮元素的化合价有升高和降低,所以是氧化还原反应,其中做氧化剂的二氧化氮有1分子,做还原剂的二氧化氮有2分子,二者比例为2:1.(Ⅱ)①铜和稀硝酸反应生成硝酸铜、一氧化氮和水,离子方程式写成:3Cu + 8H++ 2NO3 - = 3Cu2+ + 2NO↑+ 4H2O。②过量的二氧化碳和石灰水反应生成碳酸氢钙,离子方程式写成:CO2+OH- =HCO3-;③氯化铝和过量的氢氧化钠反应生成偏铝酸钠和氯化钠和水,离子方程式为: Al3+ +4OH-=AlO2-+2H2O。(Ⅲ)①二氧化硫和氧气在催化剂存在下反应生成三氧化硫,方程式为:2SO2 + O2 2SO3;②漂白液的主要成分为次氯酸钠,由氯气和氢氧化钠反应生成:Cl2+2NaOH=NaCl+NaClO+H2O;③雕刻玻璃是利用氟化氢和二氧化硅反应生成四氟化硅和水:SiO2 +4HF=SiF4↑+2H2O。
2SO3;②漂白液的主要成分为次氯酸钠,由氯气和氢氧化钠反应生成:Cl2+2NaOH=NaCl+NaClO+H2O;③雕刻玻璃是利用氟化氢和二氧化硅反应生成四氟化硅和水:SiO2 +4HF=SiF4↑+2H2O。
考点:氧化还原反应,离子方程式和化学方程式的书写。
本题难度:一般
5、选择题 含有6.02×1023个氧原子的H2SO4的物质的量是
A.1.00 mol
B.0.50 mol
C.0.25 mol
D.0.125 mol
参考答案:C
本题解析:n (H2SO4)= n(O)=
n(O)= ![]() ×
×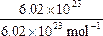 ="0.25" mol
="0.25" mol
本题难度:一般