微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应的离子方程式正确的是
A.亚硫酸氢铵和氢氧化钠的反应:NH4++OH-= NH3↑+H2O
B.足量的溴化亚铁和少量的氯气反应:2Fe2++Cl2=2Fe3++2Cl-
C.硫酸铜溶液中加过量的氨水:Cu2++2NH3・H2O==Cu(OH)2↓+2NH4+
D.Ca(HCO3)2溶液与少量NaOH溶液反应:Ca2++2HCO3-+2OH-==CaCO3↓+2H2O+CO32-
参考答案:B
本题解析:A错,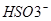 也要与氢氧化钠溶液反应;B正确;C错,氢氧化铜能与过量的氨水反应;D错,正确为Ca2++HCO3-+OH-==CaCO3↓+2H2O;
也要与氢氧化钠溶液反应;B正确;C错,氢氧化铜能与过量的氨水反应;D错,正确为Ca2++HCO3-+OH-==CaCO3↓+2H2O;
本题难度:一般
2、简答题 (14分)已知用NaAlO2制备α―Al(OH)3及能量转化关系如图:

(1)反应②的热化学方程式为 。
(2)根据上述能量转化关系,拜耳公司找到了一种简捷的从铝土矿获取Al2O3的方法,流程如下:

①物质A的化学式为 ;
②步骤Ⅲ的化学反应方程式为 ;检验步骤Ⅲ中沉淀是否洗净的方法是 ;
③步骤Ⅱ采用冷却的方法析出α―Al(OH)3,该措施的依据是 ;
④工业上可电解上述产物Al2O3以获得Al,若获得2.7kgAl,则理论上消耗A的物质的量至少为 mol。有人提出用熔融Na[AlCl4]与NaCl的混合物代替Al2O3进行电解获得Al,则阴极反应为 。
参考答案:(14分)
(1)NaAlO2(aq)+2H2O(l)
本题解析:
试题分析:(1)首先写出反应②的化学方程式并注明状态NaAlO2(aq)+2H2O(l) = NaOH(aq)+α―Al(OH)3(s)根据盖斯定律求出该反应的焓变?H=―1/2?H1 + 1/2?H3=―50kJ?mol?1,可得热化学方程式为。
(2)①Al2O3为两性氧化物,所以物质A为NaOH。
②步骤Ⅲ为Al(OH)3焙烧分解生成Al2O3,所以化学方程式为:2Al(OH)3 Al2O3+3H2O;步骤Ⅲ中沉淀如果没有洗涤干净,表面会含有Na+,所以检验方法为:取最后一次洗涤液做焰色反应,如果火焰没有黄色则已经洗净,反之则未洗净。
Al2O3+3H2O;步骤Ⅲ中沉淀如果没有洗涤干净,表面会含有Na+,所以检验方法为:取最后一次洗涤液做焰色反应,如果火焰没有黄色则已经洗净,反之则未洗净。
③根据(1)中热化学方程式可知NaAlO2水解生成α―Al(OH)3为放热反应,冷却降温促使NaAlO2水解正向移动或减小α―Al(OH)3在强碱中的溶解。
④根据化学方程式可得对应关系:Al ~ NaOH 所以n(NaOH)=2700g÷27g/mol=100mol,阴极上发生AlCl4-得电子反应,电极方程式为:AlCl4-+3e?=Al+4Cl?
考点:本题考查热化学方程式的书写、化学流程的分析、离子的检验、方程式的书写、化学计算。
本题难度:一般
3、选择题 下列离子方程式书写正确的是
A.过量的NaHSO4与Ba(OH)2溶液反应:Ba2+ + 2OH- + 2H+ + SO42- = BaSO4 ↓+ 2H2O
B.NH4HCO3溶液与过量NaOH溶液反应:NH4+ + OH- = NH3 ↑+ H2O
C.次氯酸钙溶液中通入少量二氧化碳:2ClO- + CO2 + H2O =" 2HClO" + CO32-
D.FeBr2溶液中通入过量Cl2:2Fe2+ + 2Br- + 2Cl2 = 2Fe3+ + Br2 + 4Cl-
参考答案:A
本题解析:
试题分析:选项B中氢氧化钠溶液是足量的,还有碳酸钠生成,B不正确;C中CO2不足,应该生成碳酸钙白色沉淀,C不正确;D中氯气是过量的,不符合物质的定必组成,应该是2Fe2+ +4Br- + 3Cl2 = 2Fe3+ + 2Br2 + 6Cl-,答案选A。
考点:考查离子方程式的正误判断
点评:该题是高考中的高频题,属于中等难度的试题,旨在对学生能力的培养和训练。该题需要明确判断离子方程式正确与否的方法一般,即(1)检查反应能否发生。(2)检查反应物、生成物是否正确。(3)检查各物质拆分是否正确。(4)检查是否符合守恒关系(如:质量守恒和电荷守恒等)。(5)检查是否符合原化学方程式,然后灵活运用即可。该题也有助于培养学生灵活运用基础知识分析问题、解决问题的能力。
本题难度:一般
4、填空题 (7分)有A、B、C、D四种无色溶液。它们的溶质分别是Na2CO3、Na2SO4、NaHSO4、BaCl2中的一种,为了确定各是何种溶液进行了下列实验,记录为:①A+D
参考答案:
本题解析:
本题难度:一般
5、选择题 能用离子方程式H+?+?OH?=?H2O表示的化学反应是
A.NaOH溶液和醋酸的反应
B.Ba(OH)2溶液和稀H2SO4的反应
C.NaOH溶液和硫酸氢钠溶液反应
D.氨水和稀H2SO4的反应
参考答案:C
本题解析:能用离子方程式H+ + OH = H2O表示的化学反应是,强酸和强碱反应,无沉淀,无气体生成;A.醋酸为弱酸;B.还有硫酸钡沉淀;D.氨水为弱碱,弱电解质。
本题难度:一般